题目内容
16.如图是初中化学的一些基本实验,请根据实验内容回答下列问题.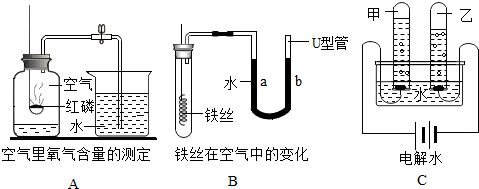
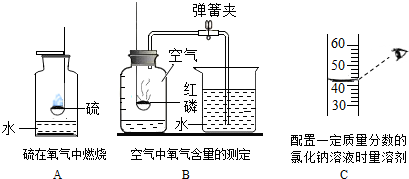
(1)A实验中发生反应的化学方程式是4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,实验结束待集气瓶冷却后,进入集气瓶中水的体积小于集气瓶容积的五分之一,可能的原因是(填一条即可)红磷不足(或装置漏气、未冷却至温室就开始读数);
(2)放置一周后,B实验观察到U型管内的现象是液面a上升,b下降;
(3)C实验中,甲试管内收集到的气体是O2,实验中发生反应的化学方程式是2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
分析 (1)根据实验的注意事项分析导致测量结果不够准确的原因;
(2)根据铁锈蚀来分析;
(3)依据电解水实验的现象、结论进行解答.通电电解水正极生成的气体是氧气,负极生成的气体是氢气,二者体积比为:1:2;
解答 解:
(1)红磷燃烧生成五氧化二磷,发生反应的化学方程式是:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;
测量的结果发现进入集气瓶中水的体积小于原瓶中空气体积的五分之一,是因为反应的红磷量不足导致氧气未被完全消耗或装置漏气或未等集气瓶彻底冷却就打开止水夹等,故填:红磷不足(或装置漏气、未冷却至温室就开始读数);
(2)铁在空气中锈蚀需消耗空气中的氧气,造成试管内的气体压强减小,所以看到U型管内a端液面上升,b端液面下降;
(3)通电电解水,一段时间后,甲试管与正极相连,生成的气体是氧气,负极生成的气体是氢气,二者的体积之比约为1:2.
实验中发生反应的化学方程式是:2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
答案:
(1)4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5;红磷不足(或装置漏气、未冷却至温室就开始读数);
(2)液面a上升,b下降;
(3)O2; 2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑;
点评 本题考查了空气中氧气含量的测定、铁的锈蚀、电解水,难度不大.考查了我们分析问题的能力.在解答时,善于抓住题目的要点,才能使解答明晰不乱.

练习册系列答案
相关题目
4.某合作学习小组讨论辨析以下说法:①用活性炭可将硬水进行软化;②煤炉火上放一盆水,就能防止一氧化碳中毒;③太阳能、风能和天然气都是可再生能源;④空气质量级别愈高,空气质量状况愈好.其中不正确的是( )
| A. | 只有②④ | B. | 只有②③④ | C. | 只有①②④ | D. | ①②③④ |
11. 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里,由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据可能是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1;
为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
【实验结论】
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
 实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.
实验室有一瓶标签受到腐蚀(如图所示)的无色溶液,老师叫各小组开展探究.【提出问题】这瓶无色溶液究竟是什么物质的溶液?
【猜想与假设】经了解得知,这瓶无色溶液原是放在存放盐溶液的柜子里,由此猜测:可能是碳酸钠、碳酸氢钠、氯化钠、硫酸钠、硝酸钠中某一种的溶液.
(1)甲同学根据标签上的组成元素认为一定不可能是氯化钠溶液.
(2)乙同学提出,碳酸氢钠、硝酸钠的溶液也不可能,他的依据可能是碳酸氢钠和硝酸钠的化学式中钠元素右下角的数字为1;
为了确定该溶液究竟是剩余两种盐的哪一种溶液,他们设计了如下实验.
| 实 验 操 作 | 实 验 现 象 |
| ①取少量该无色溶液于试管中,慢慢滴加BaCl2溶液. ②静置后,倾去上层清液,向沉淀中滴加稀盐酸. | ①产生白色沉淀. ②冒气泡,沉淀全部溶解. |
(3)该瓶无色溶液的溶质是碳酸钠.生成白色沉淀的化学方程式是Na2CO3+BaCl2=BaCO3↓+2NaCl.
12.下列属于化学变化的是( )
| A. | 水果榨汁 | B. | 汽油挥发 | C. | 粮食酿酒 | D. | 玻璃破碎 |


 A-H是初中化学常见的物质,它们之间相互转化关系如图所示,其中A用于改良酸性土壤,B是人体胃液中帮助消化的物质.
A-H是初中化学常见的物质,它们之间相互转化关系如图所示,其中A用于改良酸性土壤,B是人体胃液中帮助消化的物质.