题目内容
13.下列是初中化学常见的三个实验,回答下列问题: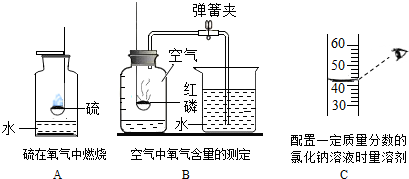
(1)A实验中,实验结束后瓶内液体的pH<7(填“>”、“<”或“﹦”).此实验集气瓶内预先装少量水的目的是防止生成的SO2气体污染环境,若用NaOH溶液代替水效果更好.
(2)请分析B中导致实验结果偏小的原因:红磷量不足(或装置气密性差、未冷却至室温就打开止水夹、没有预先在导管中装满水)(写其中一个).
(3)C实验中该操作将导致所配溶液溶质质量分数偏大(填“偏大”、“偏小”或“不变”).
(4)若用9%的氯化钠溶液100g配制质量分数为0.9%的生理盐水,需蒸馏水质量为900g.
分析 (1)硫燃烧生成的二氧化硫会与水反应生成亚硫酸,酸性溶液的pH<7;
(2)测定空气中氧气含量时导致实验结果的原因有:红磷量偏少、装置漏气、未等装置冷却就打开夹子等;
(3)俯视会导致量取液体偏小,从而使溶质的质量分数偏大;
(4)根据溶液的溶质质量分数可知一定量溶液中所含有溶质的质量,而用浓溶液配制稀溶液时溶质的质量不变,则利用溶质的质量前后相等列等式来解答.
解答 解:(1)硫燃烧生成的二氧化硫会与水反应生成亚硫酸,亚硫酸显酸性,酸性溶液的pH<7;
(2)测定空气中氧气含量时导致实验结果的原因有:红磷量偏少、装置漏气、未等装置冷却就打开夹子等;
(3)俯视会导致量取液体偏小,由溶质的质量分数=$\frac{溶质质量}{溶液质量}$×100%可知使溶质的质量分数会偏大;
(4)根据配制前后溶质的质量不变,设需蒸馏水的质量为xg,则
100g×9%═(100+x)g×0.9%
解得x═900g
故答案为:
(1)<;防止生成的SO2气体污染环境; NaOH;
(2)红磷量不足(或装置气密性差、未冷却至室温就打开止水夹、没有预先在导管中装满水);
(3)偏大;
(4)900
点评 二氧化硫是造成酸雨的原因,俯视会导致量取液体偏少,并了解测定空气中氧气含量、蒸发溶液的注意事项即可顺利解答.

练习册系列答案
相关题目
4.下列实验现象描述正确的是( )
| A. | 木炭燃烧后生成黑色固体 | |
| B. | 红磷在空气中产生大量白烟 | |
| C. | 硫燃烧后产生刺激性气味的气体 | |
| D. | 红热铁丝伸入盛有空气的集气瓶中剧烈燃烧 |
8.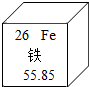 当涂县城南面的大青山不仅有“桃花山庄”等优美景区,还有着丰富的铁矿等资源.在元素周期表中,铁元素的某些信息如图所示,下列说法正确的是( )
当涂县城南面的大青山不仅有“桃花山庄”等优美景区,还有着丰富的铁矿等资源.在元素周期表中,铁元素的某些信息如图所示,下列说法正确的是( )
 当涂县城南面的大青山不仅有“桃花山庄”等优美景区,还有着丰富的铁矿等资源.在元素周期表中,铁元素的某些信息如图所示,下列说法正确的是( )
当涂县城南面的大青山不仅有“桃花山庄”等优美景区,还有着丰富的铁矿等资源.在元素周期表中,铁元素的某些信息如图所示,下列说法正确的是( )| A. | 铁元素在地壳金属元素中含量最高 | B. | 铁元素的核电荷数为26 | ||
| C. | 铁元素的原子核内质子数为56 | D. | 铁元素的相对原子质量为55.85g |
18.为了促进农作物的生长,增强抗旱能力,明明建议施用适量的磷肥,明明父母应选择的化肥是( )
| A. | KCl | B. | CO(NH2)2 | C. | Ca3(PO4)2 | D. | KNO3 |
2.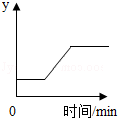 工业上常用高温煅烧石灰石的方法来制得生石灰,发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.现取一定量的石灰石样品进行煅烧(假设杂质不变),某变量y随时间的变化趋势如右图所示.则纵坐标表示的是( )
工业上常用高温煅烧石灰石的方法来制得生石灰,发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.现取一定量的石灰石样品进行煅烧(假设杂质不变),某变量y随时间的变化趋势如右图所示.则纵坐标表示的是( )
 工业上常用高温煅烧石灰石的方法来制得生石灰,发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.现取一定量的石灰石样品进行煅烧(假设杂质不变),某变量y随时间的变化趋势如右图所示.则纵坐标表示的是( )
工业上常用高温煅烧石灰石的方法来制得生石灰,发生的反应为CaCO3$\frac{\underline{\;高温\;}}{\;}$CaO+CO2↑.现取一定量的石灰石样品进行煅烧(假设杂质不变),某变量y随时间的变化趋势如右图所示.则纵坐标表示的是( )| A. | 生成CO2的体积 | B. | 生成CaO的质量 | ||
| C. | 固体中杂质的质量分数 | D. | 固体中氧元素的质量分数 |
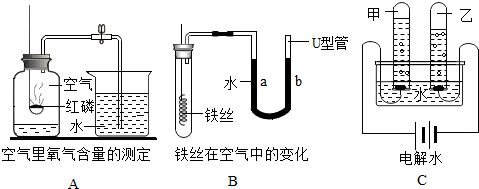
 手机在人们的生活中使用广泛,如图是充电或连接用的数据线.
手机在人们的生活中使用广泛,如图是充电或连接用的数据线.