题目内容
3.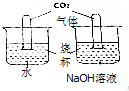 课外小组同学为探究二氧化碳的性质设计如图实验:
课外小组同学为探究二氧化碳的性质设计如图实验:(1)两个实验观察到的共同现象是试管内液面上升,产生该现象的原因是二氧化碳能溶于水,能与氢氧化钠反应.
(2)在实验中左右试管观察到的现象更明显的是右试管,原因是二氧化碳能与氢氧化钠反应,发生反应的化学方程式为CO2+2NaOH═Na2CO3+H2O.
分析 二氧化碳能溶于水、能和氢氧化钠反应生成碳酸钠和水,据此分析回答;
解答 解:(1)二氧化碳溶于水,能与氢氧化钠反应,试管中的二氧化碳会减少,从而导致试管中的气压减小,在外界大气压的作用下,试管中的液面会上升.
(2)由于二氧化碳能与氢氧化钠反应生成了碳酸钠和水,在实验中右试管观察到的现象更明显,反应的方程式是:CO2+2NaOH═Na2CO3+H2O;
故答为:(1)试管内液面上升,二氧化碳能溶于水,能与氢氧化钠反应;(2)右试管,二氧化碳能与氢氧化钠反应,CO2+2NaOH═Na2CO3+H2O.
点评 化学是一门以实验为基础的科学,实验可以帮助我们获取很多新知识,验证一些现象与结论.因此,学习化学时,不要错过每一个实验,更不要轻易放过实验中的每一个现象.

练习册系列答案
 开心蛙状元作业系列答案
开心蛙状元作业系列答案 课时掌控随堂练习系列答案
课时掌控随堂练习系列答案 一课一练一本通系列答案
一课一练一本通系列答案 浙江之星学业水平测试系列答案
浙江之星学业水平测试系列答案
相关题目
13.成语是中华文化的瑰宝.下列成语涉及化学变化的是( )
| A. | 聚沙成塔 | B. | 百炼成钢 | C. | 滴水成冰 | D. | 铁杵成针 |
11.在硝酸银、硝酸铜的混合溶液中加入一定量铁粉,反应停止后过滤,滤渣中加入盐酸,无气泡产生.有关判断正确的是( )
| A. | 滤渣中一定有银,没有铁和铜 | |
| B. | 滤渣中一定有铜,可能有铁和银 | |
| C. | 滤液中一定有硝酸亚铁、硝酸铜,没有硝酸银 | |
| D. | 滤液中一定有硝酸亚铁,可能有硝酸铜和硝酸银 |
18.随着车辆的增加,汽车尾气带给城市的污染越来越严重了,用燃气来代替燃油可以大大减少汽车尾气的污染.某市的加气站某日发生了爆炸,请你分析爆炸的原因.为防止此类事件的再次发生,请你提出一条合理化建议.
4.已知在化学反应里,元素化合价升高的物质发生氧化反应,元素化合价降低的物质发生还原反应.下列关于H2O2和MnO2制氧气的说法正确的是( )
| A. | MnO2发生了氧化反应 | |
| B. | H2O2发生了氧化反应 | |
| C. | H2O2发生了还原反应 | |
| D. | H2O2既发生了氧化反应,又发生了还原反应 |
11.已知过氧化钠的化学式为Na2 O2;则关于过氧化钠的说法正确的是( )
| A. | 由两个钠元素和两个氧元素组成 | B. | 由氧化钠分子和氧原子构成 | ||
| C. | 由钠元素和氧元素组成 | D. | 由两个钠原子和氧原子构成 |
8.武学成同学学习了锌与硫酸反应制取氢气实验后,进行铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,于是进行了如下的探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2能与氢氧化钠溶液发生反应.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】武学成同学用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助武学成同学完成如表:
【实验结论】铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸浓度达到足够大时,生成的气体产物中有二氧化硫;当硫酸溶液浓度较稀时,生成的气体产物是氢气.
【交流与反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】武学成同学又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因是形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)6H2SO4(浓)+2Fe$\frac{\underline{\;\;△\;\;}}{\;}$Fe2(SO4)3+6H2O+3SO2↑
(2)SO2可使品红溶液的红色褪去.SO2能与氢氧化钠溶液发生反应.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体产物中可能有二氧化硫.
【实验探究】武学成同学用图甲所示的装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

请帮助武学成同学完成如表:
| A中硫 酸浓度 | 实验现象 | A中生成气体成分 | |||
| B中品 红溶液 | D中品 红溶液 | 爆鸣实验 | |||
| 实验一 | 98% | 褪色 | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验二 | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | 有二氧化硫和氢气 |
| 实验三 | 25% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流与反思】(1)写出实验三中铁与硫酸反应的化学方程式:Fe+H2SO4═FeSO4+H2↑.
(2)实验一中C装置的作用是吸收二氧化硫.
【拓展延伸】武学成同学又将A装置进行了如图丙所示的改进,试分析:增加的导管下端伸入液面以下的原因是形成液封,防止生成的气体逸出;该导管所起的作用是平衡试管内外的压强,防止停止加热时液体倒吸入试管.
9.下列物质,由原子直接构成的是( )
| A. | 金刚石 | B. | 干冰 | C. | 氯化钠 | D. | 铜 |