题目内容
15.分别向NaOH、KOH溶液中滴加无色酚酞试液,酚酞试液均变成红色,仅由此实验推测使酚酞试液变红色的粒子,其结论不正确的是( )| A. | 不是K+ | B. | 可能是H2O | C. | 可能是OH- | D. | 一定是OH- |
分析 据碱溶液中的粒子是氢氧根离子使酚酞变红,排除水分子和钠离子,设计实验方案即可.
解答 解:A、分别向NaOH、KOH溶液中滴加无色酚酞试液,酚酞试液均变成红色,只有KOH溶液中含有K+,所以使酚酞试液变红色的粒子不是K+,故正确;
B、H2O显中性,不能使酚酞试液变成红色,故错误;
C、分别向NaOH、KOH溶液中滴加无色酚酞试液,都含有OH-,所以使酚酞试液变红色的粒子可能是OH-,故正确;
D、分别向NaOH、KOH溶液中滴加无色酚酞试液,都含有OH-和H2O,H2O显中性,不能使酚酞试液变成红色,所以使酚酞试液变红色的粒子是OH-,故正确;
故选:B.
点评 熟记紫色石蕊试液和无色酚酞试液遇酸碱性溶液时显示的颜色,并能举一反三,会利用性质相似的指示剂.

练习册系列答案
相关题目
5.某校化学兴趣小组就空气中氧气的含量进行实验探究:
(1)实验装置如图1所示,观察到的实验现象:红磷燃烧,放热,冒大量白烟,待装置冷却到室温
后打开止水夹,烧杯中的水倒流进集气瓶内.为了确保实验的成功,在装药品之前应该先检验装置的气密性.
(2)小组同学共同设计了如图2的两套装置,你认为合理的是A(填编号).

【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100mL)
(3)通过对实验结果的交流,大多数同学都验证出氧气约占空气体积的$\frac{1}{5}$.通过实验还可以推断集气瓶中剩余气体的性质是不能燃烧、不支持燃烧、难溶于水(写两条).
(4)同学对实验进行反思后,提出了改进方法(如图3所示),你认为改进后的优点是:环保、误差小.
(1)实验装置如图1所示,观察到的实验现象:红磷燃烧,放热,冒大量白烟,待装置冷却到室温
后打开止水夹,烧杯中的水倒流进集气瓶内.为了确保实验的成功,在装药品之前应该先检验装置的气密性.
(2)小组同学共同设计了如图2的两套装置,你认为合理的是A(填编号).

【数据分析】实验结束后,整理数据如下:(注:集气瓶容积为100mL)
| 组别 | 1 | 2 | 3 | 4 | 5 | 6 |
| 进入集气瓶中水的体积(mL) | 20 | 21 | 19 | 20 | 22 | 18 |
(4)同学对实验进行反思后,提出了改进方法(如图3所示),你认为改进后的优点是:环保、误差小.
6.“碳捕捉技术”是指通过一定的方法,将工业生产中产生的CO2分离出来进行储存和利用.常利用NaOH溶液来“捕捉”CO2,过程如图所示(部分条件及物质未标出).

下列有关该方法的叙述中正确的是( )

下列有关该方法的叙述中正确的是( )
| A. | 该方法的优点是能耗小 | |
| B. | 该方法不利于减少碳排放 | |
| C. | 整个过程中,只有一种物质可以循环利用 | |
| D. | “反应分离”中,是氢氧化钙与碳酸钠发生反应 |
3.下列是家庭厨房中的一些做法,你认为不正确的是( )
| A. | 在蒸馒头和面时,可在面中加入适量的纯碱 | |
| B. | 用食盐腌渍蔬菜 | |
| C. | 用活性炭作冰箱除味剂 | |
| D. | 夜晚发现液化气泄漏时,应立即开灯检查 |
10.铁丝在氧气中燃烧时,观察到的实验现象是( )
| A. | 发出耀眼的白光,生成白色固体 | |
| B. | 产生大量白烟,放出热量 | |
| C. | 火星四射,生成黑色固体 | |
| D. | 产生蓝紫色火焰,生成有刺激性气味的气体 |
20.下列括号中的物质是除去杂质所用的试剂,其中正确的是( )
| A. | CaO中混有少量CaCO3(水) | |
| B. | CO中混有少量CO2(NaOH溶液) | |
| C. | Na2CO3溶液中混有少量NaCl(盐酸) | |
| D. | NaOH溶液中混有少量Na2CO3溶液(CaCl2溶液) |
 我国蕴藏着丰富的海洋资源,而淡水资源短缺,需要合理利用,爱护水资源.
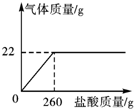
我国蕴藏着丰富的海洋资源,而淡水资源短缺,需要合理利用,爱护水资源. 2010年3月14日,某市举行了初中科学知识应用暨探究技能比赛,其中的叶脉标签制作项目是由选手在规定时间内,根据自已的创意设计,对叶脉进行染色、绘画、裁割、拼接等艺术加工.比赛时某组选手配制了200克 10%的氢氧化钠溶液,比赛结束后他们对剩余的氢氧化钠废液用盐酸进行了中和处理.
2010年3月14日,某市举行了初中科学知识应用暨探究技能比赛,其中的叶脉标签制作项目是由选手在规定时间内,根据自已的创意设计,对叶脉进行染色、绘画、裁割、拼接等艺术加工.比赛时某组选手配制了200克 10%的氢氧化钠溶液,比赛结束后他们对剩余的氢氧化钠废液用盐酸进行了中和处理.