题目内容
13.在一密闭容器里放入四种物质,使其在一定条件下充分反应,测得数据如表:| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测值 | 1 | 22 |
| A. | 未测值为3g | B. | 丙可能是催化剂 | ||
| C. | 甲与乙反应的质量比为3:14 | D. | 该反应可能是分解反应 |
分析 反应后甲物质质量减少14g,是反应物;
反应后丙物质质量不变,可能是催化剂,也可能既不是反应物,也不是生成物;
反应后丁物质质量增加17g,是生成物;
根据质量守恒定律可知,乙物质是反应物,参加反应的质量为:17g-14g=3g.
解答 解:A、未测值为:15g-3g=12g,错误;
B、反应后丙物质质量不变,可能是催化剂,正确;
C、甲与乙反应的质量比为:14g:3g=14:3,错误;
D、反应物是两种,生成物是一种,属于化合反应,错误.
故选D.
点评 学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、进行相关方面计算的基础.

练习册系列答案
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案
相关题目
3.某课外兴趣小组通过查阅资料知道过氧化钠(Na2O2)能与水反应,生成氢氧化钠和氧气,于是他们做以下探究实验.
向装有过氧化钠粉末的试管中加水,充分反应后,取试管中的少量溶液放入另一支小试管,加入几滴无色酚酞溶液,溶液变红,过了一会儿,红色又褪去了.
【提出问题】溶液为什么先变红,过一会儿,红色又褪去了呢?
【猜想】甲同学认为是氢氧化钠与空气中的二氧化碳反应的缘故.乙同学认为甲同学的猜想不正确,理由是氢氧化钠溶液与二氧化碳反应后生成的碳酸钠溶液也显碱性,也能使酚酞试液变为红色.
【查阅资料】①滴加酚酞呈红色的溶液遇到H2O2时,H2O2可破坏酚酞的结构,使酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
【猜想】通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成H2O2.
猜想B:生成的氢氧化钠溶液可能太浓.
【实验探究】请你将下列实验方案填写完整.
【得出结论】
(1)写出过氧化钠与水反应生成氢氧化钠和氧气的化学方程式:Na2O2+2H2O═2NaOH+O2↑.
(2)根据实验分析,除了上述反应外,过氧化钠与水还存在另一反应,则另一反应的化学方程式为Na2O2+2H2O=2NaOH+H2O2【拓展延伸】向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.请你对脱脂棉燃烧的原因进行分析反应中产生氧气和放出热量,使脱脂棉达到燃烧的条件.
向装有过氧化钠粉末的试管中加水,充分反应后,取试管中的少量溶液放入另一支小试管,加入几滴无色酚酞溶液,溶液变红,过了一会儿,红色又褪去了.
【提出问题】溶液为什么先变红,过一会儿,红色又褪去了呢?
【猜想】甲同学认为是氢氧化钠与空气中的二氧化碳反应的缘故.乙同学认为甲同学的猜想不正确,理由是氢氧化钠溶液与二氧化碳反应后生成的碳酸钠溶液也显碱性,也能使酚酞试液变为红色.
【查阅资料】①滴加酚酞呈红色的溶液遇到H2O2时,H2O2可破坏酚酞的结构,使酚酞在稀碱性溶液中稳定显红色,而在浓氢氧化钠等溶液中显红色后又褪色.
【猜想】通过查阅资料后,该兴趣小组对溶液的红色褪去的主要原因进行了猜想.
猜想A:过氧化钠与水反应可能生成H2O2.
猜想B:生成的氢氧化钠溶液可能太浓.
【实验探究】请你将下列实验方案填写完整.
| 猜想 | 实验操作 | 实验现象 | 结论 |
| A | 取过氧化钠与水反应的溶液放入试管中,加入适量的二氧化锰后,将 带火星的术条放在试管口 | 产生气泡,木条复燃 | 猜想A正确 |
| B | 取过氧化钠与水反应的溶液放入试管中,先加入适量的水,然后再滴 加酚酞试液 | 溶液变红,一会红色又消失 | 猜想B错误 |
(1)写出过氧化钠与水反应生成氢氧化钠和氧气的化学方程式:Na2O2+2H2O═2NaOH+O2↑.
(2)根据实验分析,除了上述反应外,过氧化钠与水还存在另一反应,则另一反应的化学方程式为Na2O2+2H2O=2NaOH+H2O2【拓展延伸】向包有过氧化钠粉末的脱脂棉上滴水,脱脂棉燃烧起来.请你对脱脂棉燃烧的原因进行分析反应中产生氧气和放出热量,使脱脂棉达到燃烧的条件.
1.已知:①能量越低的物质就越稳定,②白磷转化成红磷是放热反应.据此,下列判断或说法中正确的是( )
| A. | 在相同的条件下,红磷比白磷稳定 | |
| B. | 在相同的条件下,白磷比红磷稳定 | |
| C. | 红磷和白磷的结构不同 | |
| D. | 红磷容易发生自燃而白磷则不会自燃 |
8.硬水中一般都含有较多Ca2+、Mg2+、HCO3-等离子,在一定条件下,这些离子趋于生成溶解度更小的物质--水垢,影响工业生产的安全和产品质量.许多工业都需要软化硬水,下图为某制药厂净化生产用水的流程图.
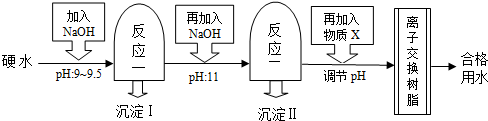
【资料搜集】查阅到下列有关物质的溶解性:
【猜想分析】(1)沉淀Ⅰ是CaCO3,沉淀Ⅱ为Mg(OH)2.
(2)反应二的化学方程式为Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3
(3)处理过程中,离子交换树脂所起的作用是除去水中的可溶性杂质
【相关链接】日常生活中所形成的水垢一定含有CaCO3和Mg(OH)2;可能含有Ca(OH)2或MgCO3.

【资料搜集】查阅到下列有关物质的溶解性:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
(2)反应二的化学方程式为Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3
(3)处理过程中,离子交换树脂所起的作用是除去水中的可溶性杂质
【相关链接】日常生活中所形成的水垢一定含有CaCO3和Mg(OH)2;可能含有Ca(OH)2或MgCO3.
5.为了对氯化钾样品(含有少量KNO3)进行组分析.甲.乙.丙.三位同学分别进行试验,他们的实验数据如下,请仔细观察分析,回答下列问题:
(1)样品中的KCl的质量分数是多少?
(2)三位同学分别把反应后的溶液过滤,哪一位同学所得的滤液是只含有一种溶质的溶液?此溶液的溶质质量分数是多少.
| 甲 | 乙 | 丙 | |
| 所取固体样品的质量(克) | 20 | 10 | 10 |
| 加入AgNO3溶液的质量(克) | 100 | 100 | 150 |
| 反应后所得的沉淀质量(克) | 14.35 | 14.35 | 14.35 |
(2)三位同学分别把反应后的溶液过滤,哪一位同学所得的滤液是只含有一种溶质的溶液?此溶液的溶质质量分数是多少.

 ”“
”“ ”“
”“ ”分别代表不同元素的原子)
”分别代表不同元素的原子)