题目内容
8.硬水中一般都含有较多Ca2+、Mg2+、HCO3-等离子,在一定条件下,这些离子趋于生成溶解度更小的物质--水垢,影响工业生产的安全和产品质量.许多工业都需要软化硬水,下图为某制药厂净化生产用水的流程图.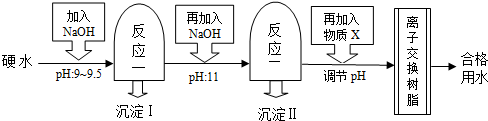
【资料搜集】查阅到下列有关物质的溶解性:
| 物 质 | Ca(HCO3)2 | Mg(HCO3)2 | Ca(OH)2 | Mg(OH)2 | CaCO3 | MgCO3 |
| 溶解性 | 可溶 | 可溶 | 微溶 | 不溶 | 不溶 | 微溶 |
(2)反应二的化学方程式为Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3
(3)处理过程中,离子交换树脂所起的作用是除去水中的可溶性杂质
【相关链接】日常生活中所形成的水垢一定含有CaCO3和Mg(OH)2;可能含有Ca(OH)2或MgCO3.
分析 (1)(2)、硬水中一般含较多的Ca2+、Mg2+、HCO3-等离子,从软化流程看,控制加入NaOH溶液的量,使其产生不同沉淀.因为这个反应的实质是一个离子反应,总向着能够减小离子浓度的方向进行.当因NaOH溶液较少即PH为9~9.5时,发生OH-与HCO3-的反应,以下反应为主:Ca(HCO3)2+2NaOH=CaCO3↓+Na2CO3 +2H2O,生成CaCO3白色沉淀,此时Mg(HCO3)2与NaOH溶液的反应受到抑制,因 MgCO3 的溶解能力比 CaCO3强.继续加入NaOH溶液即PH为11时,发生Mg2+与OH-的反应,反应方程式为:Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3 .
(3)用离子交换树脂处理,主要是通过离子交换,使溶液中的相关离子减少,达到目的.因此它除去的是可溶性的杂质.
相关链接:因硬水中离子,在一定条件下趋于生成溶解度更小的物质--水垢,由题意和溶解性表可知,CaCO3和Mg(OH)2 为不溶物,因此水垢中一定含有CaCO3和Mg(OH)2,因Ca(OH)2和MgCO3为微溶物,所以水垢中可能含有Ca(OH)2或MgCO3
解答 解:[猜想分析](1)因在一定条件下,硬水中的离子趋于生成溶解度更小的物质--水垢,由由题意和溶解性表可知:CaCO3和Mg(OH)2为不溶物.
故答案为:CaCO3;Mg(OH)2;
(2)反应一:Ca(HCO3)2+2NaOH=CaCO3↓+2H2O,Na2CO3溶液呈碱性.
反应二:Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3 .
故答案为:Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3;
(3)用离子交换树脂处理,主要是在溶液中进行离子交换.
故答案为:除去水中的可溶性杂质;
[相关链接]由题意和溶解性表可知:CaCO3和Mg(OH)2为不溶物,因此水垢中一定含有CaCO3和Mg(OH)2 ,
因Ca(OH)2和MgCO3为微溶物,所以水垢中还可能含有Ca(OH)2或MgCO3
故答案为:CaCO3;Mg(OH)2;Ca(OH)2或MgCO3.
答案:
【猜想分析】(1)CaCO3,Mg(OH)2.
(2)Mg(HCO3)2+2NaOH═Mg(OH)2↓+2NaHCO3
(3)除去水中的可溶性杂质;
【相关链接】CaCO3,Mg(OH)2.Ca(OH)2或MgCO3.
点评 该题主要联系生产实践考查硬水软化的方法.其方法除离子交换法外,还有煮沸、加热等.把握题意,了解相关物质的溶解性.

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案| A. | FeS+浓HNO3 | B. | Cu+浓HNO3 | C. | FeO+HNO3 | D. | Fe2O3+HNO3 |
| 四种物质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量(g) | 25 | 15 | 1 | 5 |
| 反应后质量(g) | 11 | 未测值 | 1 | 22 |
| A. | 未测值为3g | B. | 丙可能是催化剂 | ||
| C. | 甲与乙反应的质量比为3:14 | D. | 该反应可能是分解反应 |
 最近,西南五省市持续严重干旱,保护水环境、珍爱水资源,是每个公民应尽的责任和义务.请回答下列问题
最近,西南五省市持续严重干旱,保护水环境、珍爱水资源,是每个公民应尽的责任和义务.请回答下列问题(1)不论是河水还是海水,你认为保持水的化学性质的最小粒子是(填名称)水分子.下列能确认水是由氧元素和氢元素组成的实验是C (填序号).
A.水的蒸馏 B.水的蒸发 C.水的电解 D.水的净化
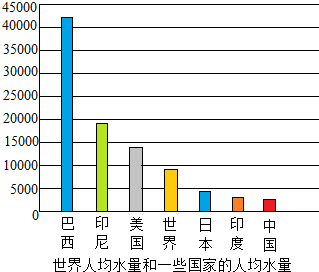
(2)如图是某些国家的人均水量和世界人均水量(m3/人).由图中可以看出我国是一个水资源严重缺乏的国家.举出你在生活中节约用水的一点做法:洗手、洗脸时随时关闭水龙头.
(3)有一杯主要含有MgCl2和CaCl2的硬水.某兴趣小组设计出软化水的部分实验方案,请你一起来完成.可供选用的物质有:Ca(OH)2溶液、NaOH溶液、饱和Na2CO3溶液、肥皂水
| 实验步骤 | 现 象 | 结论或化学方程式 |
| ①取少量水样于试管中,向其中滴加 Ca(OH)2溶液,直到不再产生沉淀 | 有白色沉淀产生 | MgCl2+Ca(OH)2═Mg(OH)2↓+CaCl2 |
| ②继续向上述试管中滴加(饱和)Na2CO3溶液,直到不再产生沉淀 | 有白色沉淀产生 | 化学方程式:CaCl2+Na2CO3=2NaCl+CaCO3↓ |
| ③过滤 | 滤液澄清 | |
| ④取上述滤液少许于试管中,滴加少量肥皂水,振荡 | 振荡产生较多泡沫 | 证明硬水已软化 |
| A. | O3属于化合物 | B. | CO2、CO、O2和O3都属于氧化物 | ||
| C. | CO2、O2中都含有氧分子 | D. | CO2、CO组成元素相同 |
 海水是名副其实的液体矿藏,平均每立方公里的海水中有3570万吨的矿物质.世界上已知的100多种元素中,80%可以在海水中找到.
海水是名副其实的液体矿藏,平均每立方公里的海水中有3570万吨的矿物质.世界上已知的100多种元素中,80%可以在海水中找到.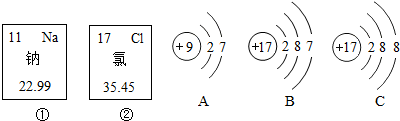
 “创新”是一个民族的灵魂,是人类发展的不竭动力.
“创新”是一个民族的灵魂,是人类发展的不竭动力.