题目内容
15.中国科学技术大学科学家在440℃和高压下,利用金属钠与二氧化碳作用得到了金刚石(化学式为C)和碳酸钠(Na2CO3),且金刚石的颗粒有望达到宝石级大小,它将给天然金刚石开采业带来极大挑战.下列说法正确的是( )| A. | 金刚石是一种金属单质 | B. | 该反应是化合反应 | ||
| C. | 该反应中生成了新的原子 | D. | 反应前后元素种类没有变化 |
分析 A、根据金刚石是碳元素形成的单质,进行分析判断.
B、金属钠与二氧化碳作用得到了金刚石和碳酸钠,进行分析判断.
C、根据化学反应遵守质量守恒定律,进行分析判断.
D、根据化学反应前后元素的种类不变,进行分析判断.
解答 解:A、金刚石是碳元素形成的单质,是一种非金属单质,故选项说法错误.
B、金属钠与二氧化碳作用得到了金刚石和碳酸钠,该反应的生成物是两种,不符合“多变一”的特征,不属于化合反应,故选项说法错误.
C、化学反应遵守质量守恒定律,反应前后原子的种类不变,故选项说法错误.
D、化学反应前后元素的种类不变,反应前后元素种类没有变化,故选项说法正确.
故选:D.
点评 本题难度不大,理解题意,掌握金属单质与化合反应的特征、质量守恒定律等是正确解答本题的关键.

练习册系列答案
相关题目
5.现有一包白色粉末,由CuSO4、NaOH、Na2CO3、CaCO3、NaCl中的两种或两种以上的物质组成.化学兴趣小组的同学们为了探究其组成,进行了如下实验:
(一)取少量白色粉末,向其中加入足量的水,充分搅拌,得无色透明溶液,则原白色粉末中一定不含有CuSO4、CaCO3.
(二)为了进一步探究白色粉末的组成,请你和兴趣小组的同学们一起完成下列探究.兴趣小组的同学们作了以下猜想:
猜想A:白色粉末为Na2CO3和NaOH的混合物
猜想B:白色粉末为Na2CO3和NaCl的混合物
猜想C:NaOH和NaCl
猜想D:白色粉末为NaOH、Na2CO3和NaCl的混合物
【设计实验】
【反思与评价】
(1)步骤2中Cu(NO3)2溶液能否用CuCl2溶液代替,为什么?不能,如果加入氯化铜溶液,氯化铜能和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,生成的氯化钠影响对氯化钠的判断
(2)写出步骤3的化学反应方程式NaCl+AgNO3═AgCl↓+NaNO3,反应类型是复分解反应.
(一)取少量白色粉末,向其中加入足量的水,充分搅拌,得无色透明溶液,则原白色粉末中一定不含有CuSO4、CaCO3.
(二)为了进一步探究白色粉末的组成,请你和兴趣小组的同学们一起完成下列探究.兴趣小组的同学们作了以下猜想:
猜想A:白色粉末为Na2CO3和NaOH的混合物
猜想B:白色粉末为Na2CO3和NaCl的混合物
猜想C:NaOH和NaCl
猜想D:白色粉末为NaOH、Na2CO3和NaCl的混合物
【设计实验】
| 实 验 操 作 | 现 象 | 结 论 |
| 1取上述无色透明溶液与试管中,加入适量的硝酸钙溶液 | 产生白色沉淀 | 猜想D成立 |
| 2过滤,取滤液少许与试管中,加入过量的Cu(NO3)2溶液 | 产生蓝色沉淀 | |
| 3静置,再向试管中加入稀硝酸和硝酸银溶液 | 产生白色沉淀 |
(1)步骤2中Cu(NO3)2溶液能否用CuCl2溶液代替,为什么?不能,如果加入氯化铜溶液,氯化铜能和氢氧化钠反应生成氢氧化铜沉淀和氯化钠,生成的氯化钠影响对氯化钠的判断
(2)写出步骤3的化学反应方程式NaCl+AgNO3═AgCl↓+NaNO3,反应类型是复分解反应.
3.下列实验现象的描述中正确的是( )
| A. | 蜡烛在氧气中燃烧时,产生水和二氧化碳 | |
| B. | 红磷在氧气中燃烧时,生成大量白色烟雾 | |
| C. | 硫粉在氧气中燃烧时,产生淡蓝色火焰,生成有刺激性气味的无色气体 | |
| D. | 水通电一段时间后,正极与负极产生的气体体积比约为1:2 |
7.草酸(H2C2O4)加热能分解.化学兴趣小组的同学对草酸受热分解的产物作如下探究:
【猜想与假设】草酸分解得到的气体产物:A.只有CO2 B.只有CO C.既有CO2,也有CO
【查阅资料】CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,立即变蓝;而CO2遇该试纸不变色
【设计方案】该兴趣小组的同学在老师的指导下,设计如图所示实验(夹持试管装置省略),通过观察下列装置中的实验现象,验证猜想.

【实验探究】请你帮助他们完成实验报告:
【讨论与反思】(1)装置B中浓硫酸的质量增加,说明草酸的分解产物还有水.
(2)根据实验结论,从环保角度考虑,实验装置中存在的不足是缺少尾气处理装置,正确的处理方法是将尾气收集到气囊中(或将尾气点燃).
【猜想与假设】草酸分解得到的气体产物:A.只有CO2 B.只有CO C.既有CO2,也有CO
【查阅资料】CO遇到浸有磷钼酸溶液的氯化钯黄色试纸,立即变蓝;而CO2遇该试纸不变色
【设计方案】该兴趣小组的同学在老师的指导下,设计如图所示实验(夹持试管装置省略),通过观察下列装置中的实验现象,验证猜想.

【实验探究】请你帮助他们完成实验报告:
| 实验步骤 | 实验现象 | 实验结论及化学方程式 |
| 点燃酒精灯加热,观 察装置C、装置D中的现象 | 装置C中试纸变蓝; 装置D中澄清石灰水变浑浊. | 草酸分解的气体产物为CO2和CO.装置D 中反应的化学方程式为Ca(OH)2+CO2=CaCO3↓+H2O. |
(2)根据实验结论,从环保角度考虑,实验装置中存在的不足是缺少尾气处理装置,正确的处理方法是将尾气收集到气囊中(或将尾气点燃).
4.我们接触到的下列各组物质,都属于纯净物的是( )
| A. | 食醋、精盐 | B. | 白酒、牛奶 | C. | 空气、氧气 | D. | 冰水混合物、氢气 |
5.下列化学现象的描述,正确的是( )
| A. | 硫在空气中燃烧发出蓝紫色火焰 | |
| B. | 铁丝在氧气中燃烧,火星四射,生成一种白色固体 | |
| C. | 木炭在氧气中燃烧比在空气中燃烧旺,发出白光,并放出热量 | |
| D. | 磷在空气中燃烧,放出大量白雾 |
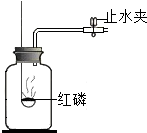 小聪和小明对竹子中气体的成分进行探究.他们把竹子浸泡在水中.在竹子上钻了一个小孔,看到有气泡从小孔中冒出.就收集了两瓶气体,第一瓶:采用如图所示的方法点燃红磷,有白烟生成.把装置放在水中,打开止水夹,进入集气瓶的水约占集气瓶体积的$\frac{1}{10}$.
小聪和小明对竹子中气体的成分进行探究.他们把竹子浸泡在水中.在竹子上钻了一个小孔,看到有气泡从小孔中冒出.就收集了两瓶气体,第一瓶:采用如图所示的方法点燃红磷,有白烟生成.把装置放在水中,打开止水夹,进入集气瓶的水约占集气瓶体积的$\frac{1}{10}$.