题目内容
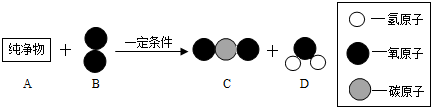
13.某班同学按如图所示的实验探究质量守恒定律.
同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中,发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.该实验中,大家进行了两次称量,有四个小组得到下列数据:
| A | B | C | D | |
| 盐酸加入Na2CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
| 盐酸加入Na2CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴人盐酸,最终天平的状态是C(填序号).选择这套装置的原因是反应在密闭容器中进行
A.左盘高 B.右盘高 C.保持平衡
(3)在图2的锥形瓶中添加氢氧化钠的原因是吸收反应生成的二氧化碳,其发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
分析 化学反应遵循质量守恒定律,即参加反应的物质的质量之和,等于反应后生成的物质的质量之和;
化学反应前后,元素的种类不变,原子的种类、总个数和质量不变.
解答 解:将盐酸加到碳酸钠粉末中,稀盐酸和碳酸钠反应生成氯化钠、水和二氧化碳,发生反应的化学方程式为:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
故填:Na2CO3+2HCl═2NaCl+H2O+CO2↑.
其中有问题的两组数据是A、D,这是因为反应后生成的二氧化碳气体逸出,质量应该减小,而A中质量不变,D中质量增大;
进行两次称量的目的是判断反应是否遵循质量守恒定律.
故填:AD;判断反应是否遵循质量守恒定律.
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴人盐酸,最终天平的状态是保持平衡;
选择这套装置的原因是反应在密闭容器中进行.
故填:C;反应在密闭容器中进行.
(3)在图2的锥形瓶中添加氢氧化钠的原因是吸收反应生成的二氧化碳,其发生反应的化学方程式为:2NaOH+CO2═Na2CO3+H2O.
故填:吸收反应生成的二氧化碳;2NaOH+CO2═Na2CO3+H2O.
点评 化学反应遵循质量守恒定律,即化学反应前后,元素的种类不变,原子的种类、总个数不变,这是书写化学方程式、判断物质的化学式、判断化学计量数、进行相关方面计算的基础.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
1.下列“家庭小实验”能成功的是( )
①用铅笔芯的粉末使锁的开启变灵活
②在煤炉上放一盆水来防止煤气中毒
③用紫甘蓝汁测定洁厕灵的酸碱性
④用食醋除去热水瓶中的水垢.
①用铅笔芯的粉末使锁的开启变灵活
②在煤炉上放一盆水来防止煤气中毒
③用紫甘蓝汁测定洁厕灵的酸碱性
④用食醋除去热水瓶中的水垢.
| A. | ①③④ | B. | ①②③ | C. | ①②④ | D. | ②③④ |
4.下列4个坐标图分别表示4个实验过程中某些质量的变化,其中正确的是( )
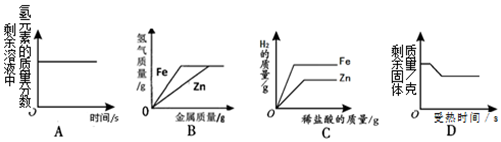

| A. | 向一定量过氧化氢溶液中加入少量二氧化锰 | |
| B. | 向相同质量与浓度的稀盐酸分别加入铁粉和锌粉 | |
| C. | 向相同质量的铁粉和锌粉中分别加入足量稀盐酸 | |
| D. | 一氧化碳与一定量氧化铁在高温条件下完全反应 |
1.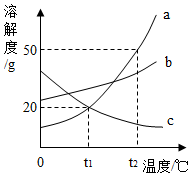 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | a物质的溶解度大于b物质的溶解度 | |
| B. | t1℃时,a、c两种物质的溶液的质量分数相等 | |
| C. | t2℃时,30ga物质加入50g水中得到80g溶液 | |
| D. | t2℃时,a、b、c三种物质的饱和溶液降温到t1℃时所得溶液质量分数由大到小的顺序是b>a>c. |
8. 已知A、B、C、D、E分别是初中化学中所学常见物质,它们之间相互转化的关系如图所示,“→”表示物质相互之间的转化,“-”表示物质之间能发生反应,A、B、C、E分别属于不同类别的化合物,A与C、E与C之间的反应产物完全相同,E在农业上可用于改良酸性土壤.下列叙述错误的是( )
已知A、B、C、D、E分别是初中化学中所学常见物质,它们之间相互转化的关系如图所示,“→”表示物质相互之间的转化,“-”表示物质之间能发生反应,A、B、C、E分别属于不同类别的化合物,A与C、E与C之间的反应产物完全相同,E在农业上可用于改良酸性土壤.下列叙述错误的是( )
 已知A、B、C、D、E分别是初中化学中所学常见物质,它们之间相互转化的关系如图所示,“→”表示物质相互之间的转化,“-”表示物质之间能发生反应,A、B、C、E分别属于不同类别的化合物,A与C、E与C之间的反应产物完全相同,E在农业上可用于改良酸性土壤.下列叙述错误的是( )
已知A、B、C、D、E分别是初中化学中所学常见物质,它们之间相互转化的关系如图所示,“→”表示物质相互之间的转化,“-”表示物质之间能发生反应,A、B、C、E分别属于不同类别的化合物,A与C、E与C之间的反应产物完全相同,E在农业上可用于改良酸性土壤.下列叙述错误的是( )| A. | 上述五种物质之间相互转化的化学反应类型中不包含置换反应 | |
| B. | D与水反应生成酸,A与水反应生成碱 | |
| C. | 可用水除去E中含有的少量A杂质 | |
| D. | A、B、E三种物质中只含有一种相同的元素 |
5.下列说法不正确的是( )
| A. | S02、CO、NO2都是造成空气污染的气体 | |
| B. | 喝汽水打嗝,是因为气体溶解度随温度升高而增大 | |
| C. | 燃烧需要同时满足三个条件,灭火只需要破坏至少一个条件即可 | |
| D. | 合金硬度一般比组成它的纯金属大 |
2.在氯化亚铁、氯化铜和氯化镁的混合溶液中加入一定量锌粉,反应停止后过滤,向滤液中插入洁净的铁丝,铁丝表面无明显变化,下列分析正确的是( )
| A. | 滤液中一定有氯化镁,可能有氯化锌和氯化亚铁 | |
| B. | 滤液中一定有氯化镁和氯化锌,可能有氯化铜 | |
| C. | 滤渣中一定有铜和铁,可能有锌 | |
| D. | 滤渣中一定有铜,可能有铁和锌 |