题目内容
1.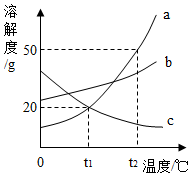 a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )
a、b、c三种固体物质的溶解度曲线如图所示,下列叙述正确的是( )| A. | a物质的溶解度大于b物质的溶解度 | |
| B. | t1℃时,a、c两种物质的溶液的质量分数相等 | |
| C. | t2℃时,30ga物质加入50g水中得到80g溶液 | |
| D. | t2℃时,a、b、c三种物质的饱和溶液降温到t1℃时所得溶液质量分数由大到小的顺序是b>a>c. |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、在一定的温度下比较不同物质的溶解度,不知道温度,不能直接比较,错误;
B、t1℃时,a、c两种物质的饱和溶液的质量分数相等,不知道溶液的状态,故不能确定溶液的溶质质量分数大小,错误;
C、t2℃时,a的溶解度为50g,故30ga物质加入50g水中只能溶解25g,得到75g溶液,错误;
D、t2℃时,a、b、c三种物质的饱和溶液降温到t1℃时,ab的溶解度都减小,会析出晶体形成该温度下的饱和溶液,根据图示可以看出,b的溶质质量分数大于a,c的溶解度随温度的降低而增大,溶液组成不变,故所得溶液质量分数由大到小的顺序是b>a>c,正确;
故选D.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列各组离子在pH=13的溶液中能大量共存,并形成无色透明溶液的是( )
| A. | Na+、K+、Cl-、CO32- | B. | H+、Na+、CO32-、SO42- | ||
| C. | NH4+、K+、NO3-、Cl- | D. | Cu2+、Ca2+、Cl-、NO3- |
10.噻吩(化学式为C4H4S)是一种应用于航空、航天等领域的新材料.下列有噻吩的说法正确的是( )
| A. | 含有2个氢分子 | B. | 碳、氢、硫三种元素质量比是4:4:1 | ||
| C. | 完全燃烧后只生成二氧化碳和水 | D. | 碳元素的质量分数最大 |
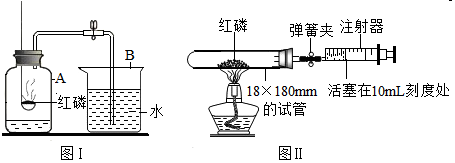
13.某班同学按如图所示的实验探究质量守恒定律.

同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中,发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.该实验中,大家进行了两次称量,有四个小组得到下列数据:
其中有问题的两组数据是AD(填序号).进行两次称量的目的是判断反应是否遵循质量守恒定律
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴人盐酸,最终天平的状态是C(填序号).选择这套装置的原因是反应在密闭容器中进行
A.左盘高 B.右盘高 C.保持平衡
(3)在图2的锥形瓶中添加氢氧化钠的原因是吸收反应生成的二氧化碳,其发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.

同学们先按图1的方式实验,将盐酸加到碳酸钠粉末中,发生反应的化学方程式为Na2CO3+2HCl═2NaCl+H2O+CO2↑.该实验中,大家进行了两次称量,有四个小组得到下列数据:
| A | B | C | D | |
| 盐酸加入Na2CO3粉末前称量/g | 85.3 | 82.8 | 84.8 | 86.5 |
| 盐酸加入Na2CO3粉末后称量/g | 85.3 | 80.6 | 83.2 | 87.8 |
(2)同学们又按照图2的方式实验,当天平平衡后,挤压胶头滴管逐滴滴人盐酸,最终天平的状态是C(填序号).选择这套装置的原因是反应在密闭容器中进行
A.左盘高 B.右盘高 C.保持平衡
(3)在图2的锥形瓶中添加氢氧化钠的原因是吸收反应生成的二氧化碳,其发生反应的化学方程式为2NaOH+CO2═Na2CO3+H2O.
10.小松同学在实验室发现一瓶久置在空气中的氢氧化钠固体,小松同学和他们小组同学探究这瓶固体变质程度,取样品13.5g于烧杯中,加入100g水使其完全溶解,逐渐加入一定质量分数的氯化钙溶液,实验数据如下:
( 1 ) 表中m的值3.0g;
(2)求样品中含氢氧化钠的质量分数?(保留到0.1%)
(3)反应前滴加氯化钙溶液的质量分数?
| 实验次数 | 第一次 | 第二次 | 第三次 |
| 加入氯化钙溶液质量/g | 20.0 | 60.0 | 80.0 |
| 生成沉淀质量/g | 1.0 | m | 3.5 |
(2)求样品中含氢氧化钠的质量分数?(保留到0.1%)
(3)反应前滴加氯化钙溶液的质量分数?
11.水常用来配制溶液.
请从27-A或27-B两题中任选1个作答,若两题均作答,按27-A计分.
请从27-A或27-B两题中任选1个作答,若两题均作答,按27-A计分.
| 27-A | 27-B |
| (1)农业上用10%~20%的NaCl溶液进行选种.现要配制15%的NaCl溶液200kg,需要NaCl和水的质量分别是30kg,170kg. (2)氯化钠是由离子(填“分子”“原子”或“离子”)构成. | (1)一定质量分数的KNO3溶液可用作无土栽培的营养液.现将100kg溶质质量分数为15%的KNO3溶液中加水400kg,溶液中溶质质量分数为3%. (2)KNO3为复合肥料,是因为KNO3为植物生长提供了必需的氮和钾元素. |
 A~I为初中化学中常见物质.已知A为金属氧化物,C为白色沉淀,D为蓝色沉淀,甲为锌粉和铁粉的混合物.(部分生成物末标出),它们之间的关系如图所示.请回答下列问题:
A~I为初中化学中常见物质.已知A为金属氧化物,C为白色沉淀,D为蓝色沉淀,甲为锌粉和铁粉的混合物.(部分生成物末标出),它们之间的关系如图所示.请回答下列问题: