题目内容
19.实验室制取氧气时,某同学取一定质量的高锰酸钾加热,记录产生氧气的质量与反应时间的关系如图1所示,请回答下列问题:
(1)请根据图中数据计算高锰酸钾的质量为多少?(写出计算过程)
(2)请在图2坐标中,画出固体中锰元素质量在t0-t5时段变化示意图.
(反应的化学方程式:2KMnO4 $\frac{\underline{\;\;△\;\;}}{\;}$ K2MnO4+MnO2+O2↑)

分析 (1)根据图1可知,氧气的质量为3.2克,根据氧气的质量,利用氧气的质量根据反应的方程式即可计算出高锰酸钾的质量;
(2)根据质量守恒定律,化学反应前后锰元素的质量不变解答.
解答 解:(1)根据图中信息可知:t0-t1固体质量不变,是因为反应还未进行;t4-t5时固体质量不变,是因为反应进行完全;
设高锰酸钾的质量是x,由图象可知该反应生成的氧气质量是3.2g;
2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑
316 32
x 3.2g
$\frac{316}{x}=\frac{32}{3.2g}$
x=31.6g
(2)31.6g高锰酸钾中锰元素的质量是31.6g×$\frac{55}{158}$×100%=11g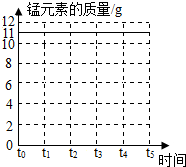
答案:
(1)高锰酸钾的质量是31.6g
(2)
点评 本题为根据化学方程式计算类问题中的基础计算,完整的计算步骤、规律的书写格式是解答此类问题时需要留意的地方.

练习册系列答案
 同步练习强化拓展系列答案
同步练习强化拓展系列答案
相关题目
9.下列各物质中,前者属于单质,后者属于混合物的是( )
| A. | 金刚石 碳酸钙 | B. | 生铁 盐酸 | C. | 液氧 大理石 | D. | 干冰 冰水混合物 |
10.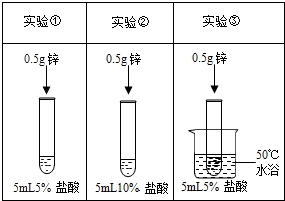 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
 为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )
为了探究影响锌与盐酸反应剧烈程度的因素,某学习小组设计了如图实验.下列说法不正确的是( )| A. | 对比实验①和②,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| B. | 对比实验①和③,可研究温度对反应剧烈程度的影响 | |
| C. | 对比实验②和③,可研究盐酸的溶质质量分数对反应剧烈程度的影响 | |
| D. | 此实验运用了控制变量法与对比实验法 |
7.元素周期表是学习和研究化学的重要工具.请根据如表(元素周期表的部分内容)回答有关问题:
(1)查出空气中含量最多元素的相对原子质量为14.01;
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | 3 Li 锂 6.941 | 4 Be 铍 9.012 | 5 B 硼 10.81 | 6 C 碳 12.01 | 7 N 氮 14.01 | 8 O 氧 16.00 | 9 F 氟 19.00 | 10 Ne 氖 20.18 |
| 3 | 11 Na 钠 22.99 | 12 Mg 镁 24.31 | 13 Al 铝 26.98 | 14 Si 硅 28.09 | 15 P 磷 30.97 | 16 S 硫 32.06 | 17 Cl 氯 35.45 | 18 Ar 氩 39.95 |
(2)在元素周期表中,同一周期中(横行)的元素,除0族(最右纵行)元素外,从左到右原子序数依次增大,原子半径逐渐减少.则原子半径:钠>镁(填“>”或“<”或“=”);
(3)第3周期第ⅥA元素的原子得到2个电子后形成了离子,该离子符号是S2-.
4.已知反应A+B=C+D且A与B参加反应的质量比为4:3,若反应后生成C和D的质量共为2.8g,则消耗的反应物B为( )
| A. | 0.3g | B. | 0.9g | C. | 1.2 g | D. | 1.6 g |
8. 2009年起,我国的防灾减灾日定为5月12日,2013年防灾减灾日的主题是“识别灾害风险,掌握减灾技能”.如图所示为学校教学楼楼道里放置的二氧化碳灭火器,下列说法错误的是( )
2009年起,我国的防灾减灾日定为5月12日,2013年防灾减灾日的主题是“识别灾害风险,掌握减灾技能”.如图所示为学校教学楼楼道里放置的二氧化碳灭火器,下列说法错误的是( )
 2009年起,我国的防灾减灾日定为5月12日,2013年防灾减灾日的主题是“识别灾害风险,掌握减灾技能”.如图所示为学校教学楼楼道里放置的二氧化碳灭火器,下列说法错误的是( )
2009年起,我国的防灾减灾日定为5月12日,2013年防灾减灾日的主题是“识别灾害风险,掌握减灾技能”.如图所示为学校教学楼楼道里放置的二氧化碳灭火器,下列说法错误的是( )| A. | 使用时,把手相当于一个省力杠杆 | |
| B. | 在钢瓶表面涂油漆的作用是防锈 | |
| C. | 铁、铜和钢属于导体,塑料和油漆属于绝缘体 | |
| D. | 加压在小钢瓶中液态二氧化碳喷出后能灭火,其原理是降低可燃物的着火点 |
9.为了测定某粉末状黄铜(铜、锌合金)样品中铜的质量分数,某化学兴趣小组取一定质量的黄铜样品放入烧杯中,再取40g稀硫酸分四次加入烧杯中,均充分反应,实验数据如下:
(1)所取黄铜样品的质量是10g;
(2)计算所用稀硫酸的溶质分数;(写出计算过程)
(3)黄铜样品中铜的质量分数为80.5%.
| 第一次 | 第二次 | 第三次 | 第四次 | |
| 加入稀盐酸的质量(g) | 10 | 10 | 10 | 10 |
| 剩余固体的质量(g) | 9.35 | 8.70 | 8.05 | 8.05 |
(2)计算所用稀硫酸的溶质分数;(写出计算过程)
(3)黄铜样品中铜的质量分数为80.5%.
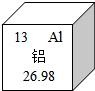 铝元素与人类关系密切. 根据如图填空:
铝元素与人类关系密切. 根据如图填空: