题目内容
9.水是生命之源,海洋是生命的摇篮.国家海洋局在2004年中国海洋环境质量公报中发布,我国全海域海水水质污染加剧.开发海洋,维持海洋的可持续发展是每个地球公民的神圣职责.请回答下面关于海洋的几个问题:(1)海水中资源丰富,含量最多的金属阳离子是Na+(填离子符号).
(2)2006年6月初,渤海海域再次发生大面积赤潮.赤潮频发的主要原因之一是由于水体富营养化造成藻类疯长.某种藻类的主要化学成分为C106H263O110N16P,成分中C、N原子的个数比为53:8;与藻类疯长的密切相关的元素是N、P(填元素符号).
(3)盐场利用海水晒盐的原理是B.(填序号)
A.氯化钠的溶解度受温度影响较大,故采取冷却热饱和溶液的方法.
B.因氯化钠溶解度受温度影响不大,故采取蒸发水分的方法.
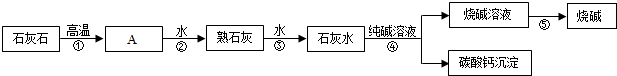
海水晒盐所得粗盐中主要含泥砂、氯化镁、氯化钙等杂质,现对其进行提纯,主要操作流程如下:
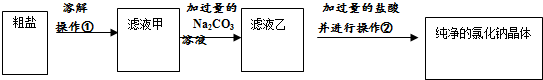
操作①的名称是过滤,操作②的名称是蒸发.
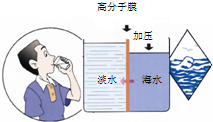
(4)海水淡化是国际上研究的热点问题,我国科学家在利用高分子膜进行海水淡化的研究上取得了一些成绩.如下图,右侧为海水,左侧为经过一段时间后由右侧经高分子膜渗透得到的淡水,分析高分子膜必须具有的性质是高分子膜允许水分子通过,而其他离子无法通过.
分析 (1)根据海水中的主要物质分析;
(2)根据化学式中元素个数计算方法计算,再结合赤潮的原因;
(3)根据氯化钠的溶解度受温度影响分析,再结合实验室常见操作分析;
(4)结合题意,利用所学知识作答.
解答 解:(1)因为海水中所含化学物质最多的是H2O,其次就是NaCl,
故答案为:Na+;
(2)因为藻类的主要化学成分为C106H263O110N16P,所以成分中C、N原子的个数比=106:16=53:8,N、P、K是植物生长的营养元素,
故答案为:53:8;N、P.
(3)因为氯化钠的溶解度受温度影响比较小,所以应用蒸发结晶的方法使其析出来,所以应选择B;
由粗盐制得精盐的流程为:粗盐经溶解、过滤后得到NaCl、MgCl2、CaCl2的混合溶液(即滤液甲),向其中加入过量的NaOH溶液(即A溶液),经过滤此时得到Mg(OH)2、Ca(OH)2沉淀和NaCl溶液、剩余的NaOH溶液(即滤液乙),在向其中家过量的盐酸(即B溶液),中和多余的NaOH溶液,使其转化为NaCl溶液,因为盐酸受热易挥发,所以加热蒸发最后的溶液即可制得纯净的食盐.
故选B; 过滤; 蒸发;
(4)观察题中所给图可知高分子膜允许水分子通过,而其他离子无法通过,
故答案为:高分子膜允许水分子通过,而其他离子无法通过.
点评 当物质的溶解度受温度影响不大时用加热蒸发的方法使其结晶出来;当物质的溶解度受温度影响比较大时用冷却热饱和溶液的方法使其结晶出来.

练习册系列答案
 高效智能课时作业系列答案
高效智能课时作业系列答案
相关题目
11.某白色固体A可能含有碳酸钠、氯化钡(水溶液呈中性)、氢氧化钠中的一种或几种,进行如下实验:
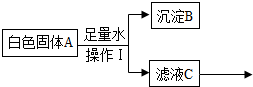
完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.

完成下列填空:
①根据上述实验分析,A中一定含有的物质是碳酸钠、氯化钡,写出生成B的化学方程式:Na2CO3+BaCl2═BaCO3↓+2NaCl.
②为进一步确定固体A中可能存在的物质,对滤液C进行实验,完成如表.
| 实验操作 | 现象 | 结论 |
| 向滤液C中加入足量的氯化钡溶液,充分反应后,静置,取上层清液滴加无色酚酞 | 无色酚酞变红色 | A中有氢氧化钠 |
4.某校化学实验小组在做铁与硫酸溶液反应的实验时,发现生成的气体有刺激性气味,他们进行了以下探究.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)铁在加热条件下与浓硫酸发生反应:
Fe+6H2SO4(热、浓)═Fe2(SO4)3+3SO2↑+6H2O
(2)SO2可使品红溶液的红色褪去.
(3)SO2是一种能与碱溶液发生反应的非金属氧化物.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体中可能有二氧化硫.
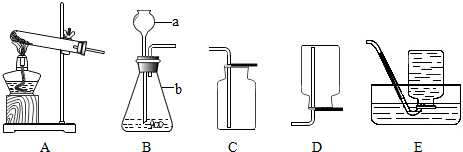
【实验探究】小组同学用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

三组实验后将记录的实验现象和对A中气体成分的分析制成表格,请补充未填入的实验现象.
【实验结论】根据上表可以得出的实验结论是铁与不同浓度的硫酸溶液反应,生成的气体产物可能不同,当硫酸 浓度达到足够大时,生成的气体产物中有二氧化硫.
【交流反思】实验Ⅰ中D装置的作用是检验二氧化硫是否被氢氧化钠溶液完全吸收.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,该装置的优点是能够形成液封,防止生成的气体逸出并且平衡试管内外的压强,防止停止加热时液体倒吸入试管.
【提出问题】铁与硫酸溶液反应生成的气体为什么有刺激性气味?
【查阅资料】(1)铁在加热条件下与浓硫酸发生反应:
Fe+6H2SO4(热、浓)═Fe2(SO4)3+3SO2↑+6H2O
(2)SO2可使品红溶液的红色褪去.
(3)SO2是一种能与碱溶液发生反应的非金属氧化物.
【进行猜想】铁与不同浓度的硫酸溶液反应,生成的气体中可能有二氧化硫.
【实验探究】小组同学用图甲所示装置进行实验,并将E中收集到的气体进行如图乙所示的爆鸣实验.

三组实验后将记录的实验现象和对A中气体成分的分析制成表格,请补充未填入的实验现象.
| A中浓硫酸浓度 | 实验现象 | A中生成 气体成分 | |||
| B中品红溶液 | D中品红溶液 | 爆鸣实验 | |||
| 实验Ⅰ | 98% | ① | 不褪色 | 无爆鸣声 | 只有SO2 |
| 实验Ⅱ | 45% | 稍有褪色 | 不褪色 | 有爆鸣声 | ② |
| 实验Ⅲ | 20% | 不褪色 | 不褪色 | 有爆鸣声 | 只有H2 |
【交流反思】实验Ⅰ中D装置的作用是检验二氧化硫是否被氢氧化钠溶液完全吸收.
【拓展延伸】小明又将A装置进行了如图丙所示的改进,该装置的优点是能够形成液封,防止生成的气体逸出并且平衡试管内外的压强,防止停止加热时液体倒吸入试管.
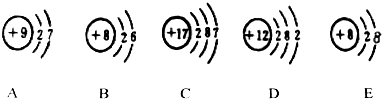
14.对于Cl和Cl-的说法,不正确的是( )
| A. | 属于同一种元素 | B. | 质子数相同 | ||
| C. | 核外电子数相同 | D. | 具有相同的电子层数 |