题目内容
14.某化学兴趣小组利用废旧干电池回收填料中的二氧化锰并探究二氧化锰的化学性质.查阅资料:废旧干电池填料的主要成分为二氧化锰、碳粉、氯化铵和氯化锌等,其中氯化铵、氯化锌可溶于水.

(1)操作1的名称是过滤(填操作名称),该操作中玻璃棒的作用是引流.
(2)灼烧滤渣1的目的是除去二氧化锰中混有的碳粉;写出该反应的化学方程式C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2.
(3)将二氧化锰加入过氧化氢溶液中,反应前后质量和化学性质不变.
(4)实验室浓盐酸可与二氧化锰在加热条件下反应生成氯气、二氧化锰和水,请写出该反应的化学方程式MnO2+2HCl=MnCl2+2H2O+Cl2↑.
分析 (1)根据操作1和操作2分离混合物的状态及过滤可用于难溶性固体和可溶性固体的分离进行分析;
(2)根据碳粉灼烧后变为二氧化碳除掉;
(3)催化剂在反应前后质量和化学性质不变;
(4)根据化学方程式的书写方法考虑.
解答 (1)把不溶性物质与液体分离的方法是过滤,过滤时玻璃棒的作用是引流;
(2)碳粉灼烧后变为二氧化碳除掉逸散到空气中,所以灼烧滤渣1的目的是除去二氧化锰中混有的碳粉;反应物是碳和氧气,生成物是二氧化碳,所以方程式是:C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;
(3)将二氧化锰加入过氧化氢溶液中,二氧化锰是催化剂,在反应前后质量和化学性质不变;
(4)反应物是二氧化锰和盐酸,生成物是氯化锰、水和氯气,所以方程式是:MnO2+2HCl=MnCl2+2H2O+Cl2↑.
故答案为:(1)过滤;引流;(2)除去二氧化锰中混有的碳粉;C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2;(3)质量和化学性质;(4)MnO2+2HCl=MnCl2+2H2O+Cl2↑.
点评 本题考查了废电池的物质的回收的探究,知识点较多,属于化学实验基本实验技能的考查,要求在平时的学习中要注意掌握常见的化学操作及其原理,熟练运用.

练习册系列答案
相关题目
2.常温下,实验室用过氧化氢制取氧气时,没有加催化剂,其结果是( )
| A. | 不影响化学反应速率 | B. | 反应速度慢.产生氧气的质量减少 | ||
| C. | 不产生氧气 | D. | 产生氧气的质量不变,反应速度慢 |
9.下列实验方案设计中,正确的是( )
| A. | 除去NaCl中少量的Na2CO3杂质,先加入足量稀硝酸,再蒸发结晶 | |
| B. | 实验室制备干燥、纯净的氢气,用锌与浓盐酸反应,产生的气体经浓硫酸干燥后收集 | |
| C. | 实验室里除去CO2中的CO,可以用点燃的方法 | |
| D. | 检验可燃性气体中是否含有氢元素,在其燃烧火焰上方罩上干冷的烧杯,观察有无水雾 |

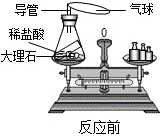 小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题:
小明设计了一个实验来探究质量守恒定律.如图所示,反应前天平平衡,他取下此装置(装置气密性良好)将其倾斜,使稀盐酸(HCl)和大理石(主要成分是碳酸钙)接触,生成氯化钙、二氧化碳气体和水,待充分反应后,气球膨胀,再将装置放回天平左盘,此时他发现天平的指针向右偏转了.请回答下列问题: 铝在工业和日常生活中应用广泛,请回答
铝在工业和日常生活中应用广泛,请回答

 根据元素周期表及原子结构示意图,回答下列问题
根据元素周期表及原子结构示意图,回答下列问题
 ,其结构决定了氧在反应中,容易得到电子,能与C、Mg、CH4等物质反应,从而决定了O2可用作助燃剂.
,其结构决定了氧在反应中,容易得到电子,能与C、Mg、CH4等物质反应,从而决定了O2可用作助燃剂.