题目内容
16.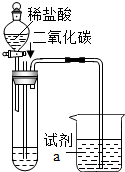 化学实验小组在做二氧化碳和氢氧化钠溶液反应的趣味实验.查阅资料如下:
化学实验小组在做二氧化碳和氢氧化钠溶液反应的趣味实验.查阅资料如下:表1 NaOH、Na2CO3和NaCl在水中的溶解度(20℃)
| T/℃ | NaOH | Na2CO3 | NaCl |
| 20 | 109 | 21.8 | 36.0 |
| T/℃ | NaOH | Na2CO3 | NaCl |
| 20 | 17.3 | - | 0.1 |
Ⅰ.向烧杯中加入试剂a.向2支试管中分别加入20mL一定溶质质量分数的氢氧化钠的水溶液(试管1)和20mL饱和的氢氧化钠的乙醇溶液(试管2).
Ⅱ.分别通入适量的二氧化碳.
Ⅲ.再分别滴加稀盐酸.
关于该实验有以下分析与解释:
①通入适量的二氧化碳时试管2中NaOH与CO2反应的化学方程式为2NaOH+CO2═Na2CO3↓+H2O.
②烧杯中出现浑浊,则试剂a为澄清石灰水.
③通入二氧化碳后,试管1、2中的现象明显相同.
④通过上述实验,对于没有明显现象的反应,可以通过证明有新物质的生成来证明反应的发生.
⑤新物质的生成,可以利用化学性质来证明,也可以用其物理性质证明.
以上说法正确的是( )
| A. | ①②③④ | B. | ②③④⑤ | C. | ①②④⑤ | D. | ①②③⑤ |
分析 根据氢氧化钠和碳酸钠在水中和乙醇中的溶解度以及氢氧化钠与二氧化碳反应生成碳酸钠和水、氢氧化钙与二氧化碳反应生成碳酸钙和水分析,
解答 解:①氢氧化钠与二氧化碳反应生成碳酸钠和水,氢氧化钠在乙醇中为易溶,生成的碳酸钠在乙醇中几乎不溶,所以试管2中有白色晶体析出.化学方程式为:2NaOH+CO2═Na2CO3↓+H2O;故正确;
②氢氧化钙与二氧化碳反应生成碳酸钙沉淀和水,所以烧杯中出现浑浊,则试剂a为石灰水,故正确;
③氢氧化钠在水中溶解度较大,消耗二氧化碳多,氢氧化钠在乙醇中溶解度较小,消耗二氧化碳少,并且生成的碳酸钠在乙醇中几乎不溶,所以试管1中无现象,试管2中有白色晶体析出.故错误;
④氢氧化钠与二氧化碳反应生成碳酸钠和水,没有明显现象,可以通过证明有碳酸钠生成来证明反应的发生.故正确;
⑤新物质的生成,可以利用化学性质来证明(例如试管1中加盐酸),也可以用其物理性质证明(例如试管2中,在乙醇溶液中碳酸钠几乎不溶,有白色晶体析出).故正确;
故选:C.
点评 本题主要考查二氧化碳的化学性质及应用,掌握碱的化学性质;学会分析反应现象和本质的联系.

练习册系列答案
 提分百分百检测卷系列答案
提分百分百检测卷系列答案 宝贝计划期末冲刺夺100分系列答案
宝贝计划期末冲刺夺100分系列答案 能考试全能100分系列答案
能考试全能100分系列答案
相关题目
4.下列物质由原子构成的是( )
| A. | 金刚石 | B. | 蛋白质 | C. | 氯化钠 | D. | 液态水 |
11.溶解是生活中常见的现象,下表是KNO3、NaCl在不同温度下的溶解度.请回答:
(1)20℃时,NaCl的溶解度是36g.
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
(5)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则是蒸发前原溶液是不饱和(填“饱和”或“不饱和”)溶液.n的数值是9.

| 温度(℃) | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| KNO3/g | 13.3 | 20.9 | 32 | 45.8 | 64 | 85.5 | 110 | 138 | 169 | 202 | 246 |
| NaCl/g | 35.7 | 35.8 | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
(2)40℃时,将70gKNO3固体加入100g水中,充分搅拌,形成的溶液质量为163.9g.
(3)60℃时,KNO3的饱和溶液中含有少量NaCl,通过降温结晶方法获得较纯净的KNO3晶体.
(4)根据表内数据可知,KNO3和NaCl在某一温度时具有相同的溶解度X,则X的取值范围是36g~36.3g.
(5)某温度下,将一定质量的KNO3溶液进行恒温蒸发结晶,实验过程如图所示,则是蒸发前原溶液是不饱和(填“饱和”或“不饱和”)溶液.n的数值是9.

1.溶解是生活中常见的现象,不同物质在水中的溶解能力不同.
①下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水).
Ⅰ.20℃时,将20gNaCl放入50g水中,所得溶液的质量是68g.
Ⅱ.从NaCl溶液中得到NaCl晶体的方法是蒸发结晶.
②用硫酸铜进行如图所示的实验,完成下列填空(用编号表示).

Ⅲ.所得三种溶液中:一定属于饱和溶液的是A,溶液中溶质质量分数的大小关系是C>B>A.
①下表是KNO3、NaCl在不同温度下的溶解度(单位:g/100g水).
| 温度(℃) | 0 | 20 | 40 | 60 | 80 | 100 |
| KNO3 | 13.3 | 31.6 | 63.9 | 110 | 169 | 246 |
| NaCl | 35.7 | 36.0 | 36.6 | 37.3 | 38.4 | 39.8 |
Ⅱ.从NaCl溶液中得到NaCl晶体的方法是蒸发结晶.
②用硫酸铜进行如图所示的实验,完成下列填空(用编号表示).

Ⅲ.所得三种溶液中:一定属于饱和溶液的是A,溶液中溶质质量分数的大小关系是C>B>A.
8.如下图是实验室制取气体的常用仪器.请根据要求填空:
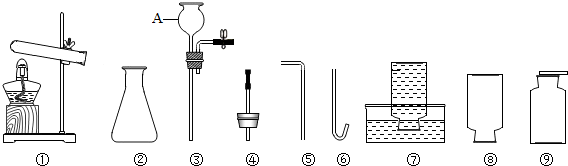
(1)图中仪器名称是②锥形瓶,⑧集气瓶.
(2)小宝同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择上图中的仪器①④⑤⑨(或①④⑥⑦)(填序号,以下同),其化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;验证瓶中氧气已集满的方法是将带火星的木条放到瓶口,如果木条复燃,则已收满.
(3)小茹同学用锌和稀硫酸制取H2,同时生成硫酸锌,则应选择上图中②③⑥⑦装置,其化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(4)小佳同学查阅资料得到制取硫化氢气体的如下信息,请回答下列问题:
①制取硫化氢不可以(填“可以”或“不可以”)采用装置①,理由是反应不需要加热;
②制取硫化氢可以(填“可以”或“不可以”)采用装置②和③,理由是反应物是固体和液体,且反应不需要加热.

(1)图中仪器名称是②锥形瓶,⑧集气瓶.
(2)小宝同学用氯酸钾和二氧化锰制取并收集一瓶氧气,应选择上图中的仪器①④⑤⑨(或①④⑥⑦)(填序号,以下同),其化学方程式为:2KClO3$\frac{\underline{MnO_2}}{△}$2KCl+3O2↑;验证瓶中氧气已集满的方法是将带火星的木条放到瓶口,如果木条复燃,则已收满.
(3)小茹同学用锌和稀硫酸制取H2,同时生成硫酸锌,则应选择上图中②③⑥⑦装置,其化学方程式为:Zn+H2SO4═ZnSO4+H2↑.
(4)小佳同学查阅资料得到制取硫化氢气体的如下信息,请回答下列问题:
| 气体 | 实验药品 | 反应条件 | 气体物理性质 |
| H2S | 硫化亚铁固体与稀硫酸 | 不需加热 | 无色,密度比空气大,可溶于水 |
②制取硫化氢可以(填“可以”或“不可以”)采用装置②和③,理由是反应物是固体和液体,且反应不需要加热.
 如图是 A、B、C三种物质的溶解度曲线.请回答:
如图是 A、B、C三种物质的溶解度曲线.请回答: