题目内容
1.某化学兴趣小组学习碱的性质后,到实验室做实验.小明将二氧化碳通入氢氧化钠溶液后无明显现象,然后向得到的溶液中滴加CaCl2溶液,产生白色沉淀;小杰做的实验和小明一样,但没有出现白色沉淀.他们为了查明原因,查阅资料:①CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,反应的化学方程式:CO2+2NaOH=Na2CO3+H2O,Na2CO3+CO2+H2O=2NaHCO3;②Ca(HCO3)2溶于水,溶液呈碱性;③CaCl2溶液呈中性:④Na2CO3、NaHCO3溶液都呈碱性,都能与酸反应;⑤铝、锌、铁、铜的盐溶液与NaHCO3溶液混合会产生沉淀.他们对CO2与NaOH溶液反应后,溶液中溶质是什么进行探究.
【猜想与假设】猜想①Na2CO3;猜想②NaHCO3;猜想③Na2CO3、NaOH;猜想④Na2CO3、NaOH、NaHCO3.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| (1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入稀盐酸 | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑. |
| (2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加无色酚酞试液. | 产生白色沉淀;溶液变红. | 猜想③成立 |
分析 【猜想与假设】根据题意,CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,进行分析解答.
【实验探究】(1)根据碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀,碳酸氢钠能与稀盐酸反应生成二氧化碳气体,进行分析解答.
(2)根据碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀,氢氧化钠溶液呈碱性,能使无色酚酞试液变红解答.
【继续探究】根据参加反应的氢氧化钠的质量计算反应的二氧化碳的质量,进一步确定反应后溶液中的溶质.
解答 解:【猜想与假设】CO2与NaOH反应的产物与反应物的量有关,少量CO2得到Na2CO3,过量CO2得到NaHCO3,故猜想④应为Na2CO3、NaOH、NaHCO3的混合物.
【实验探究】(1)碳酸钠能与氯化钙溶液反应生成碳酸钙沉淀,取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡,无明显现象,说明不含碳酸钠;再加入稀盐酸,有气泡产生,说明含碳酸氢钠,则猜想②成立,碳酸氢钠能与稀盐酸反应生成氯化钠、水和二氧化碳,反应的化学方程式为NaHCO3+HCl=NaCl+H2O+CO2↑.
(2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡,产生白色沉淀,说明反应后的溶液中有碳酸钠;过滤,取滤液于另一支试管中,滴加无色酚酞试液,溶液变红,溶液呈碱性,说明反应后的溶液中有NaOH,猜想③成立.
【继续探究】设反应中消耗二氧化碳的质量为为x,
2NaOH+CO2═Na2CO3+H2O
80 44 106
4g x
$\frac{80}{4g}=\frac{44}{x}$
x=2.2g
二氧化碳过量,说明含有碳酸氢钠生成,
充分反应后,所得溶液的溶质是碳酸钠和碳酸氢钠.
故答案为:【猜想与假设】Na2CO3、NaOH、NaHCO3.
【实验探究】
| 实验操作 | 实验现象 | 结论 |
| (1)取适量反应后的溶液于试管中,加入适量的CaCl2溶液,振荡;再加入 稀盐酸 | 无明显现象;有气泡产生. | 猜想②成立,反应的化学方程式 NaHCO3+HCl=NaCl+H2O+CO2↑. |
| (2)取适量反应后的溶液于试管中,加入过量的CaCl2溶液,振荡;过滤,取滤液于另一支试管中,滴加 无色酚酞试液. | 产生白色沉淀; 溶液变红. | 猜想③成立 |
点评 本题通过提出问题、做出猜想、设计实验方案、进行实验和反思评价等环节,体现了科学探究的一般过程.本题型也是近几年的中考热点之一,本考点主要出现在实验题中.

 学习实践园地系列答案
学习实践园地系列答案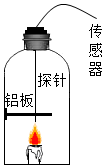 蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:
蜡烛(主要含C、H、O元素)在密闭容器中熄灭的原因是什么?燃烧的产物是什么?小敏认为蜡烛熄灭的原因是燃烧消耗完了容器内的氧气,并对燃烧产物提出猜想:①燃烧的产物可能有CO2;
②燃烧的产物可能有H2O;
除了上述猜想,你的猜想,燃烧的产物可能有CO.
实验一:在密闭容器中点燃蜡烛至熄灭,抽取10毫升密闭容器中的气体,注入到试管中的饱和澄清石灰水中,发现石灰水始终没有变浑浊.从实验的科学性考虑下一步是BC(选填字母)
A.直接得到燃烧产物中没有CO2的结论
B.再多抽取一些气体注入到试管中的石灰水中
C.增加饱和澄清石灰水的质量.
实验二:在老师的指导下,利用多功能传感器进行有关量的测量,装置如图所示.实验结束后,铝板表面有黑色固体颗粒,同时传感器采得实验前后的有关数据如表所示:
| 相对湿度 | 氧气含量 | 二氧化碳含量 | 一氧化碳含量 | |
| 蜡烛点燃前 | 48.4% | 18.7% | 0.058% | 0 |
| 蜡烛熄灭后 | 71.6% | 15.6% | 3.643% | 0.018% |
| A. | 空气由空气分子构成 | B. | 稀有气体可用作电光源 | ||
| C. | N2可作食品保鲜的保护气 | D. | O2、N2的体积比约为1:4 |
【探究目的】确定反应后溶液的酸碱性
【猜想与假设】反应后溶液呈碱性,也可能呈酸性,也可能呈中性.
【实验验证】
| 实验操作 | 实验现象 | 实验结论 |
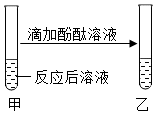 | 无色酚酞溶液变红色; | 溶液呈碱性,使其呈碱性的微粒是氢氧根离子; |
| 无色酚酞溶液不变色 | 溶液呈酸性或中性; |
| 实验操作 | 实验现象 | 实验结论 |
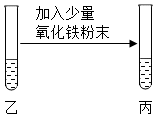 | 粉末部分或全部消失,溶液变为黄色 | 溶液呈酸性,反应的化学方程式是Fe2O3+6HCl═2FeCl3+3H2O; |
| 无明显变化 | 溶液呈中性; |
| A. | 地球是一个水球,有90%的面积被水覆盖 | |
| B. | 陆地淡水几乎占地球总水量的$\frac{3}{4}$ | |
| C. | 冰融化为水后,体积变小 | |
| D. | 健康的成年人每天一般约摄水25升水 |
| A. |  测溶液pH | B. |  闻气味 | C. |  熄灭酒精灯 | D. |  取用药品 |
 如图是初中化学常见的几种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去).A、B、C、D、E、F分别是两种常见的酸、单质,可榕性钡盐溶液,金属氧化物和非金属氧化物中的一种.用“-”表示两种物质之间可以发生化学
如图是初中化学常见的几种物质间的转化及反应关系(部分反应物或生成物及反应条件已略去).A、B、C、D、E、F分别是两种常见的酸、单质,可榕性钡盐溶液,金属氧化物和非金属氧化物中的一种.用“-”表示两种物质之间可以发生化学