题目内容
5. 小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.
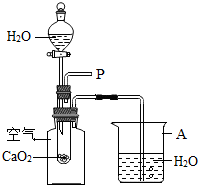
小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.(1)为研究鱼塘中大量气泡是何种气体所致,小明使用如图所示的装置进行实验,打开分液漏斗的活塞,控制滴加水的速度,观察到试管内有气泡产生,用带火星的木条靠近P处,木条复燃,说明生成的气体是氧气.由此可知养鱼师傅向鱼塘中撒过氧化钙的目的是向鱼塘中补充氧气.
(2)根据质量守恒定律,小明认为过氧化钙与过量水反应还应产生某种含有钙元素的产物.开始小明假设该产物为CaO,但通过思考他很快否定了原先的假设,并重新假设生成的含钙产物为Ca(OH)2.请解释小明否定原假设建立新假设的理由:根据质量守恒定律,因反应物中含有氢元素,所以应有含有氢元素的生成物产生.
(3)小明在实验时观察到烧杯中有气泡产生,由此他还得出了什么结论?CaO2与H2O的反应是放热反应.
分析 根据已有的知识进行分析解答,鱼呼吸作用时需要氧气,足量的氧气是保证鱼存活的条件之一;在化学反应中遵循质量守恒定律,即反应前后元素的种类不变,原子的种类、个数不变;气体受热时体积膨胀,据此解答即可.
解答 解:(1)鱼塘中的鱼较多,呼吸作用时需要大量的氧气,向鱼塘中撒过氧化钙时,能和水反应生成氧气,供给鱼呼吸.
故填:向鱼塘中补充氧气.
(2)根据质量守恒定律,因反应物中含有氢元素,所以应有含有氢元素的生成物产生,氢氧化钙中含有氢元素,氧化钙中不含有氢元素,所以生成物除氧气外,还生成氢氧化钙.
故填:根据质量守恒定律,因反应物中含有氢元素,所以应有含有氢元素的生成物产生.
(3)烧杯中有气泡产生,说明反应是放热的,放出的热量使广口瓶中的温度升高,空气膨胀,从导管口逸出,产生气泡.
故填:CaO2与H2O的反应是放热反应.
点评 化学实验现象是化学实验最突出、最鲜明的部分,也是进行分析推理得出结论的依据,掌握物质的性质和相互之间的反应关系,有助于提高观察实验、进行实验的能力.所以,对化学实验不仅要认真观察,还应掌握设计实验、观察实验现象的方法.

练习册系列答案
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案
相关题目
15.某温度下,a克溶质溶解在a克水中恰好饱和,此溶质在该温度下的溶解度是( )
| A. | 100克 | B. | a克 | C. | 2a克 | D. | 50克 |
16. 甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )
甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )
 甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )
甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )| A. | BaCl2、HCl | B. | H2SO4、Ba(NO3)2 | C. | MgSO4、NaCl | D. | H2SO4、MgCl2 |
13.对于化学反应:4P+5O2$\frac{\underline{\;点燃\;}}{\;}$2P2O5,下列说法正确的是( )
①参加反应的物质是磷和氧气;②反应前后分子总数不变;③反应前后元素的种类不变;④反应前后原子的种类和数目不变;⑤反应前后物质的总质量不变;⑥反应前后元素的化合价不变.
①参加反应的物质是磷和氧气;②反应前后分子总数不变;③反应前后元素的种类不变;④反应前后原子的种类和数目不变;⑤反应前后物质的总质量不变;⑥反应前后元素的化合价不变.
| A. | ①②⑥ | B. | ②③④⑤ | C. | ①②③⑤ | D. | ①③④⑤ |
10.已知相同温度下,在溶液中进行的化学反应的快慢(化学反应速率)既与单位体积内参加反应的溶质质量(微粒数目)有关,也与参加反应的固体跟溶液的接触面积有关,某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可以加快氢气的生成速率,请回答下列问题
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑.
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验,将表中所给的混合溶液(混合前后溶液的体积变化忽略不计)分别加入到6个盛有过量等量锌粒(锌粒与溶液的接触面积相同)的反应瓶中,收集产生的气体,记录获得同样多的气体所需的时间
①请完成此实验设计,其中:V1=30;V6=12;
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
(1)上述实验中发生反应的化学方程式有Zn+CuSO4=ZnSO4+Cu、Zn+H2SO4=ZnSO4+H2↑.
(2)为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验,将表中所给的混合溶液(混合前后溶液的体积变化忽略不计)分别加入到6个盛有过量等量锌粒(锌粒与溶液的接触面积相同)的反应瓶中,收集产生的气体,记录获得同样多的气体所需的时间
| 实验混合溶液 | A | B | C | D | E | F |
| 28%稀盐酸/mL | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO溶液/mL | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| HO/mL | V7 | V8 | V9 | V10 | 8 | 0 |
②该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高,但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降,请分析氢气生成速率下降的主要原因加入的CuSO4溶液超过一定量时,生成的单质Cu会沉积在Zn的表面,降低了Zn与溶液的接触面积.
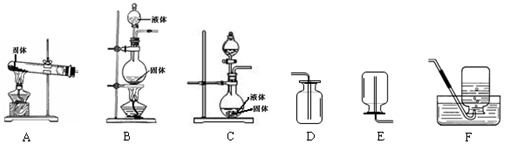
17.小岳同学在学习气体的性质时,阅读到以下资料:制取气体的发生装置取决于反应前的药品状态和反应条件,收集气体的装置取决于气体能否与水反应、在水中的溶解性以及该气体相对于空气的密度大小.现有甲、乙、丙三种气体的反应前的物品状态、反应条件以及有关性质如下表,有关装置如图.
请你回答下列问题:
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气.根据所查资料,制取氨气应选择的发生和收集装置分别是A和E(填序号).
| 气体 | 反应前的药品状态 | 反应条件 | 气体性质 |
| 甲 | 固体+液体 | 常温 | 不与水反应,不易溶于水,密度比空气大 |
| 乙 | 固体+固体 | 加热 | 能与水发生反应,极易溶于水,密度比空气小 |
| 丙 | 固体+液体 | 加热 | 能与水发生反应,能溶于水,密度比空气大 |

请你回答下列问题:
(1)能用发生装置A 制取的气体是乙(填“甲”、“乙”或“丙”);
(2)实验室要制取和收集甲气体,请写出一个符合要求的化学方程式2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;
(3)相同条件下,氨气(NH3)的密度比空气小,且易溶于水,其水溶液称为氨水;加热氯化铵和氢氧化钙固体混合物可制取氨气.根据所查资料,制取氨气应选择的发生和收集装置分别是A和E(填序号).
14.化学实验活动课上,同学们利用如图实验探究氢氧化钙的性质.
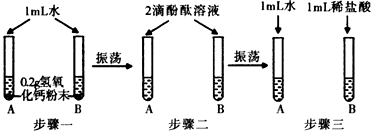
(1)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是步骤二中A中的溶液变红色.
(2)以上实验结束后,B试管中的固体消失,溶液澄清并呈无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:CaCl2、HCl 猜想二:CaCl2、Ca(OH)2、HCl 猜想三:CaCl2
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
写出加入锌粒后发生反应的化学方程式Zn+2HCl═ZnCl2+H2↑.
【讨论交流】小红同学所做的实验结束后,试管中所得溶液一定含有的溶质是氯化钙、氯化锌(除指示剂外)

(1)上述三个步骤的A试管中的固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是步骤二中A中的溶液变红色.
(2)以上实验结束后,B试管中的固体消失,溶液澄清并呈无色.
【提出问题】步骤三B试管的溶液中,除指示剂外,溶质的成分还有什么?
【猜想】猜想一:CaCl2、HCl 猜想二:CaCl2、Ca(OH)2、HCl 猜想三:CaCl2
【小组讨论】同学们经过讨论得出猜想二一定是错误的.
【实验探究】小红同学利用了下面的实验验证了猜想一.
| 实验操作 | 实验现象 | 实验结论 |
| 取步骤三B试管中溶液样品倒入盛有锌粒的试管中 | 产生气泡 | 猜想一正确 |
【讨论交流】小红同学所做的实验结束后,试管中所得溶液一定含有的溶质是氯化钙、氯化锌(除指示剂外)
 如图所示,玻璃管中有色液体的左右移动可反映出瓶内气体温度的变化.当向盛有水的试管中加入少量的固体氢氧化钠时,发现有色液体向右移动,这说明氢氧化钠固体溶于水放热.而当向盛有水的试管中加入少量的硝酸铵时,发现有色液体向左移动,这又说明了硝酸铵固体溶于水吸热.
如图所示,玻璃管中有色液体的左右移动可反映出瓶内气体温度的变化.当向盛有水的试管中加入少量的固体氢氧化钠时,发现有色液体向右移动,这说明氢氧化钠固体溶于水放热.而当向盛有水的试管中加入少量的硝酸铵时,发现有色液体向左移动,这又说明了硝酸铵固体溶于水吸热.