题目内容
20. 如图所示,玻璃管中有色液体的左右移动可反映出瓶内气体温度的变化.当向盛有水的试管中加入少量的固体氢氧化钠时,发现有色液体向右移动,这说明氢氧化钠固体溶于水放热.而当向盛有水的试管中加入少量的硝酸铵时,发现有色液体向左移动,这又说明了硝酸铵固体溶于水吸热.
如图所示,玻璃管中有色液体的左右移动可反映出瓶内气体温度的变化.当向盛有水的试管中加入少量的固体氢氧化钠时,发现有色液体向右移动,这说明氢氧化钠固体溶于水放热.而当向盛有水的试管中加入少量的硝酸铵时,发现有色液体向左移动,这又说明了硝酸铵固体溶于水吸热.
分析 氢氧化钠固体溶于水放热,溶液的温度升高;
硝酸铵固体溶于水吸热,溶液的温度降低.
解答 解:氢氧化钠固体溶于水放热,会使集气瓶中的气体受热膨胀,有色液体向右移动;硝酸铵固体溶于水吸热,导致集气瓶中的空气遇冷收缩,有色液体向左移动.
故填:氢氧化钠固体溶于水放热;硝酸铵固体溶于水吸热.
点评 有些物质溶于水后,会使溶液的温度改变.如:溶于水后使溶液温度升高的:氢氧化钠固体、浓硫酸、氧化钙固体;
物质溶于水后使溶液温度降低的.如硝酸铵固体.

练习册系列答案
 鸿图图书寒假作业假期作业吉林大学出版社系列答案
鸿图图书寒假作业假期作业吉林大学出版社系列答案
相关题目
10.下列现象或方法,不只与空气中的水蒸气有关的是( )
| A. | 浓硫酸露置于空气中会增重、变稀 | |
| B. | 固体烧碱要密封保存 | |
| C. | 夏季空调冷气吹到的地方可看到有“冷气雾” | |
| D. | 打开浓盐酸的瓶盖,瓶口产生白雾 |
8.化学工业的飞速发展给我们的生活带来了许多便利,但是一些不合理行为也给环境带来了严重的污染.下列行为不会污染环境的是( )
| A. | 回收废旧塑料减少白色污染 | |
| B. | 提倡使用私家车出行 | |
| C. | 大量使用化肥农药提高农作物的产量 | |
| D. | 将工厂排放废弃的烟囱加高 |
15.如图中的符号表示2个氧分子的是( )
| A. |  | B. |  | C. |  | D. |  |
12.下列物质的用途主要是由其化学性质决定的是( )
| A. | 氧气可用于生物呼吸 | B. | 活性炭可用于除去冰箱中的异味 | ||
| C. | 铜丝可用作导线 | D. | 干冰可用于人工降雨 |
9.某兴趣小组同学对实验室制备氧气的催化剂进行如下探究.
【提出问题】
①二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
【查阅资料】
研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
实验室用氯酸钾制取氧气,如果不用二氧化锰作催化剂,最好选用的氧化物是氧化铜.
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同.Ⅲ中X的值应为3.0,实验I和Ⅲ比较可证明CuO改变KClO3分解的速率.
【结论】
氧化铜也能做氯酸钾分解的催化剂,实验Ⅲ中的化学反应方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
(注意:若答对该题奖励4分,化学十九总分不超过60分)
【实验反思】
(1)实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
(2)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量相同时间内收集氧气的体积大小;
②测量收集相同体积氧气所需要时间长短.
【提出问题】
①二氧化锰常作为氯酸钾分解制取氧气的催化剂,那其他氧化物是否也能催化氯酸钾分解呢?是否比二氧化锰催化效果更好?
【查阅资料】
研究表明,许多金属氧化物对氯酸钾的分解(分解时放出热量)有催化作用.分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
| 氧化铁 | 氧化铝 | 氧化铜 | 氧化镁 | |
| 开始反应 | 420 | 515 | 305 | 490 |
| 剧烈反应 | 490 | 540 | 350 | 545 |
【设计并完成实验】
Ⅰ.将3.0g氯酸钾放在试管中加热
Ⅱ.将3.0g氯酸钾与1.0g二氧化锰混合均匀加热
Ⅲ.将Xg氯酸钾与1.0g氧化铜混合均匀加热
【实验现象分析】
将实验Ⅲ反应后的固体加水溶液、过滤、洗涤、干燥,若称量得到1.0g黑色粉末,再将黑色粉末和Xg氯酸钾混合加热,现象与实验Ⅲ相同.Ⅲ中X的值应为3.0,实验I和Ⅲ比较可证明CuO改变KClO3分解的速率.
【结论】
氧化铜也能做氯酸钾分解的催化剂,实验Ⅲ中的化学反应方程式为2KClO3$\frac{\underline{\;CuO\;}}{△}$2KCl+3O2↑.
(注意:若答对该题奖励4分,化学十九总分不超过60分)
【实验反思】
(1)实验Ⅱ和Ⅲ对比的目的是CuO对KClO3催化效果是否比MnO2好.
(2)在相同温度下比较两组实验产生氧气的快慢,通常可采用的方法有:
①测量相同时间内收集氧气的体积大小;
②测量收集相同体积氧气所需要时间长短.
10.下列关于溶解度的说法正确的是( )
| A. | 100克水最多可溶解36克氯化钠,则氯化钠的溶解度为36克 | |
| B. | 20℃时100克饱和氯化钠溶液中含有26克氯化钠,则20℃时氯化钠的溶解度为26克 | |
| C. | 25℃时100克水中溶解了35克氯化钠,则25℃时氯化钠的溶解度为35克 | |
| D. | 20℃时50克水中最多溶解氯化钠18克,则20℃时氯化钠的溶解度为36克 |
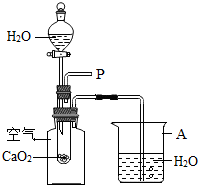 小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.
小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.