题目内容
16. 甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )
甲、乙两化工厂分布如图所示.箭头代表水流方向.如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7、且只含有少量NaCl.则b处水中含有的物质应是下列那一组?( )| A. | BaCl2、HCl | B. | H2SO4、Ba(NO3)2 | C. | MgSO4、NaCl | D. | H2SO4、MgCl2 |
分析 根据题意,如果在a处取得水样经检测只有少量OH-、SO42-.在c处取得水样经检测pH=7,说明显中性,且只含有少量NaCl,据此结合复分解反应的条件,进行分析判断.
解答 解:在a处取得水样经检测只有少量OH-、SO42-,在c处取得水样经检测pH=7,说明显中性,且只含有少量NaCl,说明发生反应后溶液中的溶质只有氯化钠.
A、氯化钡中的钡离子与硫酸反应生成硫酸钡沉淀,盐酸与氢氧根离子反应生成水,能使c处取得水样经检测pH=7,且只含有少量NaCl,故选项正确.
B、Ba(NO3)2中的钡离子与硫酸反应生成硫酸钡沉淀,但同时会生成可溶性的硝酸盐,会使c处中含有硝酸盐,故选项错误.
C、MgSO4中的镁离子与氢氧根结合生成氢氧化镁沉淀,但没有将硫酸根离子沉淀,会使c处中含有硫酸盐,故选项错误.
D、MgCl2中的镁离子与氢氧根结合生成氢氧化镁沉淀,但没有将硫酸根离子沉淀,会使c处中含有硫酸盐,故选项错误.
故选:A.
点评 本题难度不大,熟练掌握复分解反应发生的条件、溶液的酸碱性和溶液pH大小之间的关系是正确解答本题的关键.

练习册系列答案
 课程达标测试卷闯关100分系列答案
课程达标测试卷闯关100分系列答案 新卷王期末冲刺100分系列答案
新卷王期末冲刺100分系列答案 全能闯关100分系列答案
全能闯关100分系列答案
相关题目
6. 课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
 课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )
课堂上老师利用如图装置测定空气中氧气的含量.在红磷燃烧后恢复到室温,打开弹簧夹时,发现进入广口瓶的液体体积小于广口瓶容积的$\frac{1}{5}$.造成这一现象的原因可能是( )| A. | 外界大气压偏大 | B. | 实验装置可能漏气 | ||
| C. | 实验中所取的红磷过量 | D. | 集气瓶中预先未加入一定量的水 |
7.由石灰石、水、纯碱为原料制烧碱,发生反应的类型不包括( )
| A. | 分解反应 | B. | 置换反应 | C. | 化合反应 | D. | 复分解反应 |
4.下列实验操作正确的是( )
| A. |  点燃酒精灯 | B. |  检查气密性 | C. |  稀释浓硫酸 | D. |  收集氢气 |
1.如图是甲、乙两位同学一起在实验室进行的氢氧化钠与盐酸反应的实验.

根据如图实验,请你与甲、乙同学一起完成下列探究:

根据如图实验,请你与甲、乙同学一起完成下列探究:
| 探究环节 | 甲同学的探究 | 乙同学的探究 |
| 提出问题 | A3溶液为什么不变红? | B3溶液中溶质成分是什么?(酚酞不计) |
| 作出猜想 | 实验过程中,酚酞变质了 | 猜想一:NaCl 猜想二:NaCl、HCl |
| 实验验证 | (1)取少量A3溶液于另一试管中,向其中滴加NaOH溶液,溶液变红,说明甲同学的猜想不成立(填“成立”或“不成立”). (2)你认为,在常温下A2溶液测出的pH应<(填“大于”、“=”、“<”)7. | 取少量B3溶液加入盛有少量铁粉的试管中,观擦到有无色气体产生,固体逐渐减少,溶液由无色变为浅绿色,有关化学方程式是Fe+2HCl═FeCl2+H2↑. 据此,你认为乙同学的猜想二(填“一”或“二”)成立. |
| 交流反思 | (1)甲、乙同学的实验中,反应均涉及到的化学方程式是HCl+NaOH═NaCl+H2O. (2)A3溶液未变红,你认为原因是A2溶液中盐酸较多,加入的NaOH溶液未将其完全中和. (3)甲、乙同学经过实验对比探究,一致认为做化学实验时应注意药品用量的控制. | |
8.化学工业的飞速发展给我们的生活带来了许多便利,但是一些不合理行为也给环境带来了严重的污染.下列行为不会污染环境的是( )
| A. | 回收废旧塑料减少白色污染 | |
| B. | 提倡使用私家车出行 | |
| C. | 大量使用化肥农药提高农作物的产量 | |
| D. | 将工厂排放废弃的烟囱加高 |
6.药品分类存放是实验室管理的基本要求.某校实验室的药品柜里已存放的部分药品如下:
(1)若要在每个柜子门上贴上物质类别的标签,则②号柜的标签上应写酸.(“酸”“碱”“氧化物”“盐”或“金属”)
(2)上述柜子中的有些物质间能发生置换反应.请从柜中选择两种物质,写出它们之间发生置换反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
| 药品柜编号 | ① | ② | ③ | ④ | ⑤ |
| 药品 | 氢氧化钠 氢氧化钙 | 盐酸 硫酸 | 二氧化锰 氧化铜 | 氯化钠 硫酸铜 | 锌粒 铜片 |
(2)上述柜子中的有些物质间能发生置换反应.请从柜中选择两种物质,写出它们之间发生置换反应的化学方程式Zn+H2SO4=ZnSO4+H2↑.
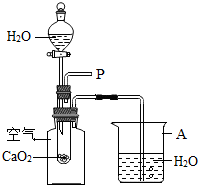 小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.
小明在回家的途中经过一鱼塘边时,发现养鱼师傅向鱼塘中撒一种微黄色的固体,鱼塘中顿时产生大量气泡,经咨询得知,这种固体的主要成分是过氧化钙(CaO2),请你与小明共同探究.