��Ŀ����
15��Ϊ�˲ⶨijƷ��ʳ�ô�����̼���Ƶ�����������С��ȡ10��ʳ�ô�����Ʒ��������������������Ϊ10%��ϡ���ᣬ������ͼ��ʵ�飬ʵ��ǰ������װ���л���ͨһ�������������Ʒ����ȫ�����Ȼ��ƣ�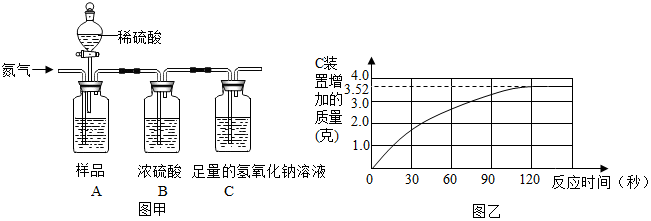
��1��ʵ�������Aװ��ͨ��һ���������Ŀ�����ž�װ���ڿ���������װ����ԭ�п����е�CO2��ʵ��ĸ��ţ�
��2��Bװ�õ�����������ˮ���������������̼��
��3�����Ŵ�����Ʒ��ϡ���ᷴӦ��Cװ�����ӵ������仯�����ͼ����ʾ�����ʳ�ô�����̼���Ƶ����������Ƕ��٣�
��̼������ϡ���ᷴӦ�Ļ�ѧ����ʽ��Na2CO3+H2SO4=Na2SO4+H2O+CO2����
���� ��1�������к��ж�����̼����Բⶨ����������ţ�
��2������Ũ���������ˮ�Է�����
��3��̼���ƺ�ϡ���ᷴӦ���������ơ�ˮ�Ͷ�����̼�����ݱ����ṩ�����ݺͷ�Ӧ�Ļ�ѧ����ʽ���Խ�����ط���ļ��㣮
��� �⣺��1��ʵ��ǰ������Aװ��ͨ��һ���������Ŀ�����ž�װ���ڿ���������װ����ԭ�п����е�CO2��ʵ��ĸ��ţ�
����ž�װ���ڿ���������װ����ԭ�п����е�CO2��ʵ��ĸ��ţ�
��2��Bװ�õ�����������ˮ���������������̼��
�������ˮ���������������̼��
��3����̼��������Ϊx��
�ɱ������ݿ��ƣ���Ӧ���ɶ�����̼��������3.52g��
Na2CO3+H2SO4�TNa2SO4+H2O+CO2����
106 44
x 3.52g
$\frac{106}{x}=\frac{44}{3.52g}$��
x=8.48g��
���ʳ�ô�����̼���Ƶ����������ǣ�$\frac{8.48g}{10g}$��100%=84.8%��
�𣺸�ʳ�ô�����̼���Ƶ�����������84.8%��
���� ������Ҫ����ѧ�����û�ѧ����ʽ���м�����ƶϵ�����������ʱҪע��淶�Ժ�ȷ�ԣ�

 ������ӱ������ͯ������ϵ�д�
������ӱ������ͯ������ϵ�д� A�ӽ��� ϵ�д�
A�ӽ��� ϵ�д� ȫ�Ų��Ծ�ϵ�д�
ȫ�Ų��Ծ�ϵ�д�| ҩƷ���� | �� | �� | �� | �� | �� |
| ҩƷ | �������� �������� | ���� ���� | �������� ����ͭ | �Ȼ��� ����ͭ | п�� ͭƬ |
��2�����������е���Щ���ʼ��ܷ����û���Ӧ����ӹ���ѡ���������ʣ�д������֮�䷢���û���Ӧ�Ļ�ѧ����ʽZn+H2SO4=ZnSO4+H2����
| �������� | ̼���� | ʯ�� | |
| ����X | ���������� | �������� | ��Һ��� |
| A�� | �������� | B�� | ����ͭ | C�� | ���� | D�� | �Ȼ��� |
| A�� | 100��ˮ�����ܽ�36���Ȼ��ƣ����Ȼ��Ƶ��ܽ��Ϊ36�� | |
| B�� | 20��ʱ100�˱����Ȼ�����Һ�к���26���Ȼ��ƣ���20��ʱ�Ȼ��Ƶ��ܽ��Ϊ26�� | |
| C�� | 25��ʱ100��ˮ���ܽ���35���Ȼ��ƣ���25��ʱ�Ȼ��Ƶ��ܽ��Ϊ35�� | |
| D�� | 20��ʱ50��ˮ������ܽ��Ȼ���18�ˣ���20��ʱ�Ȼ��Ƶ��ܽ��Ϊ36�� |
��֪ʶ�طš�
�������˳��K Ca Na Mg Al ZnFeSn Pb��H��CuHgAg Pt Au���������ں�������д��Ӧ������Ԫ�ط��ţ���
���������롿
����һ��Cr��Fe��Cu
�������Fe��Cu��Cr
��������Fe��Cr��Cu��
���������ϡ�
�ٸ�������ɫ�й���Ľ������ڿ���������������ɿ���ʴ�����ܵ�����Ĥ��
�ڸ�����ϡ���ᷴӦ��������ɫ�������Ǹ���CrSO4����Һ��
�������ʵ�顿
����ȡ��״��С��ͬ�����ֽ���Ƭ����ɰֽ��ĥ��������ȡ��֧�Թܣ��ֱ���������ͬ��ϡ���ᣬ�����ֽ���Ƭ�ֱ�����Թ��У��۲�����
| ʵ�� | �Թ�1 | �Թ�2 | �Թ�3 |
| ʵ����� |  |  |  |
| ʵ������ | ��Ƭ����������ݽ�������Һ��Ϊdz��ɫ | ��Ƭ����������ݽϿ죬��Һ��Ϊ��ɫ | ���������� |
��1�������õ�����ȷ�����Dz���һ��
��2��ʵ��ǰ��ɰֽ��ĥ����Ƭ��Ŀ���dz�ȥ�������������Ĥ��
��֪ʶ���á�
��1������ƬͶ��FeSO4��Һ�У���Ӧ�ܣ���ܡ����ܡ������У�
��2��д��̽����������ͭ�Ļ��ǿ�������������Լ����������Һ����������ͭ��Һ������ͭ������������Һ����ÿһ����������Լ���
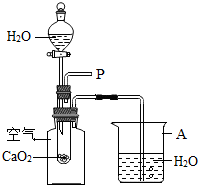 С���ڻؼҵ�;�о���һ������ʱ����������ʦ������������һ����ɫ�Ĺ��壬�����ж�ʱ�����������ݣ�����ѯ��֪�����ֹ������Ҫ�ɷ��ǹ������ƣ�CaO2����������С����ͬ̽����
С���ڻؼҵ�;�о���һ������ʱ����������ʦ������������һ����ɫ�Ĺ��壬�����ж�ʱ�����������ݣ�����ѯ��֪�����ֹ������Ҫ�ɷ��ǹ������ƣ�CaO2����������С����ͬ̽����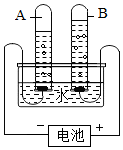 ��ͼ�ǵ��ˮ��ʵ��װ�ã�ͨ������缫�϶�������ų���
��ͼ�ǵ��ˮ��ʵ��װ�ã�ͨ������缫�϶�������ų���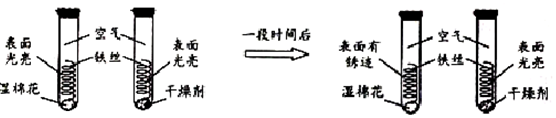
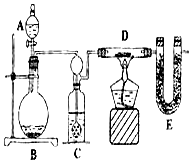 ijͬѧΪ�˲ⶨˮ���⡢����Ԫ�ص������ȣ����������ʵ�飬ʵ��װ����ͼ��
ijͬѧΪ�˲ⶨˮ���⡢����Ԫ�ص������ȣ����������ʵ�飬ʵ��װ����ͼ��