题目内容
2.下列叙述遵守质量守恒定律的是( )| A. | 镁带在空气中燃烧后,生成物质量大于镁带的质量,此反应不遵守质量守恒定律 | |
| B. | 10g酒精和10g水混和,可得到20g酒精溶液 | |
| C. | 6g硫和6g氧气反应,可生成12g二氧化硫 | |
| D. | 12g碳和12g氧气反应,可得到24g二氧化碳 |
分析 质量守恒定律是物质在发生化学变化中表现出来的一种规律,适用于化学变化;物质发生物理变化,则不适用于质量守恒定律来解释;是化学变化时也要对反应前后物质的质量关系进行计算判断,即反应时是否符合固定的质量比,据此分析解答即可
解答 解:A、镁带在空气中燃烧后生成物质量大于镁带的质量,是因为镁带与氧气反应生成了氧化镁,氧化镁的质量等于参加反应的镁带和氧气的质量和,故生成物的质量大于镁带的质量,故反应遵守质量守恒定律,此项错误;
B、10g水和10g酒精混合得20g酒精溶液不是化学变化,故选项不正确;
C、硫和氧气反应的化学方程式为:S+O2$\frac{\underline{\;点燃\;}}{\;}$SO2可知,硫、氧气、二氧化硫的质量比为1:1:2,则6g硫与6g氧气反应生成12g二氧化硫,符合质量守恒定律;故选项正确.
D、12g碳与12g氧气充分反应氧气有剩余,故不能生成24g二氧化碳,故选项错误;
故选C
点评 根据质量守恒定律,在化学反应中参加反应前各物质的质量总和等于反应后生成各物质的质量总和,掌握化学变化和物理变化的判别是解题的关键

练习册系列答案
相关题目
13.已知某两种物质在光照条件下能发生化学反应,其微观示意图如下:(一种小球代表一种原子)

则下列说法正确的是( )

则下列说法正确的是( )
| A. | 该反应属于置换反应 | B. | 图示中共有4种分子 | ||
| C. | 该反应属于化合反应 | D. | 该反应中有两种单质 |
10.农业科技人员和农民建议:在利用温室生产时,可向温室内通入适量的二氧化碳.这是因为( )
| A. | CO2可使害虫窒息死亡从而防治病虫害 | |
| B. | 施用CO2可促进植物的光合作用 | |
| C. | CO2可产生温室效应从而提高室温 | |
| D. | CO2能灭火,施用后可防止火灾 |
17.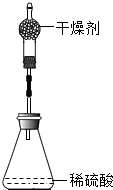 为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:
为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:
若不考虑干燥剂吸收空气中的水蒸气,计算:
(1)根据质量守恒定律求生成氢气的质量0.4g.
(2)该合金中锌的质量分数.
 为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:
为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
(1)根据质量守恒定律求生成氢气的质量0.4g.
(2)该合金中锌的质量分数.
14.分别将下列各组物质同时加入到足量水中,最终能得到无色、透明溶液的是( )
| A. | NaOH H2SO4 BaCl2 | B. | NaOH CuSO4 NaCl | ||
| C. | HNO3 KNO3 NaOH | D. | Na2SO4 FeCl3 KCl |
 张南同学在家里发现一盒××胃药,如图所示标签,从说明书上得知此胃药含治疗胃酸过多药物的成分,已知胃药的有效成分是AI(OH)3,和NaHCO3中的一种物质.张南同学设计了一个实验,请你推测这种药物的成分,并回答有关问题:
张南同学在家里发现一盒××胃药,如图所示标签,从说明书上得知此胃药含治疗胃酸过多药物的成分,已知胃药的有效成分是AI(OH)3,和NaHCO3中的一种物质.张南同学设计了一个实验,请你推测这种药物的成分,并回答有关问题: