题目内容
5. 张南同学在家里发现一盒××胃药,如图所示标签,从说明书上得知此胃药含治疗胃酸过多药物的成分,已知胃药的有效成分是AI(OH)3,和NaHCO3中的一种物质.张南同学设计了一个实验,请你推测这种药物的成分,并回答有关问题:
张南同学在家里发现一盒××胃药,如图所示标签,从说明书上得知此胃药含治疗胃酸过多药物的成分,已知胃药的有效成分是AI(OH)3,和NaHCO3中的一种物质.张南同学设计了一个实验,请你推测这种药物的成分,并回答有关问题:(1)设计实验:
取8片药品,放在研钵中研碎,加入到质量为50g烧杯中,再加入56.5g某质量分数的稀盐酸,恰好完全反应后,测得烧杯及杯内物总质量为124.3g.(假定药片的其它成分不与盐酸反应,也不溶于水)
(2)回答问题:
①胃药中有效成分的化学式是NaHCO3;
②请写出实验中发生反应的化学方程式NaHCO3+HCl═NaCl+H2O+CO2↑;
③请根据已知条件列出求解参加反应的稀盐酸中溶质质量(x)的比例式$\frac{36.5}{x}=\frac{44}{2.2g}$;
④请计算反应后所得溶液中溶质的质量分数39.2%.
分析 (1)根据取8片药品,放在研钵中研碎,加入到质量为50g烧杯中,再加入56.5g某质量分数的稀盐酸,恰好完全反应后,测得烧杯及杯内物总质量为124.3g.溶液质量减少,可知胃药中有效成分是碳酸氢钠;
8片该药品质量与稀盐酸的质量之和,再减去反应后烧杯内物质的总质量,即为生成的二氧化碳的质量;
根据二氧化碳的质量可以求出参加反应的稀盐酸中溶质质量,生成氯化钠的质量.
解答 解:
①AI(OH)3,与盐酸反应生成氯化铝和水,溶液质量不减少;碳酸氢钠与盐酸反应,生成氯化钠、水和二氧化碳,溶液质量会减少;故胃药中有效成分碳酸氢钠,化学式是NaHCO3;
②碳酸氢钠与盐酸反应,生成氯化钠、水和二氧化碳,发生反应的化学方程式为:NaHCO3+HCl═NaCl+H2O+CO2↑;
③8片该药品的质量为8片×2.5g/片=20g
生成二氧化碳的质量为:20g+50g+56.5g-124.3g=2.2g.
设参加反应的稀盐酸中溶质质量为x,生成氯化钠的质量为y,
NaHCO3+HCl═NaCl+H2O+CO2↑,
36.5 58.5 44
x y 2.2g
$\frac{36.5}{x}=\frac{44}{2.2g}$
$\frac{58.5}{y}=\frac{44}{2.2g}$
y=29.25g
反应后所得溶液中溶质的质量分数=$\frac{29.25g}{124.3g-50g}×$100%≈39.2%
答案:
①NaHCO3;
②NaHCO3+HCl═NaCl+H2O+CO2↑;
③$\frac{36.5}{x}=\frac{44}{2.2g}$;
④39.2%.
点评 本题主要考查根据化学方程式进行计算,书写化学方程式时要注意规范性.本题容易出错的地方是反应后所得溶液的计算.

 补充习题江苏系列答案
补充习题江苏系列答案 学练快车道口算心算速算天天练系列答案
学练快车道口算心算速算天天练系列答案| A. | 镁带在空气中燃烧后,生成物质量大于镁带的质量,此反应不遵守质量守恒定律 | |
| B. | 10g酒精和10g水混和,可得到20g酒精溶液 | |
| C. | 6g硫和6g氧气反应,可生成12g二氧化硫 | |
| D. | 12g碳和12g氧气反应,可得到24g二氧化碳 |
| A. | X元素可以与W元素形成XW2和XW3两种化合物 | |
| B. | Y元素的单质一定条件下可以与O2、N2、CO2反应 | |
| C. | Z原子的最外层电子数为4,形成化合物时一般为+4价 | |
| D. | X与Y、Z与W都属于同一周期 |
| A. | 1:1:1:1 | B. | 2:3:2:2 | C. | 24:27:65:56 | D. | $\frac{1}{12}$:$\frac{1}{9}$:$\frac{2}{65}$:$\frac{1}{28}$ |
| 选项 | 需鉴别的物质 | 加试剂或方法 | |
| 方法1 | 方法2 | ||
| A | 稀盐酸、氯化钾溶液 | 无色酚酞、看颜色 | 加入铁粉、看气泡 |
| B | 生石灰、熟石灰 | 两种物质分别溶于水 | 向两种物质中分别加入稀盐酸 |
| C | 蒸馏水、酒精 | 分别点燃 | 品尝 |
| D | 厕所清洁剂、厨房洗涤剂 | 用pH试纸测定它们的pH | 分别加入少量石蕊试液 |
| A. | A | B. | B | C. | C | D. | D |
| A. |  将NaCI倒入量筒中配制溶液 | B. | 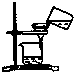 过滤 | ||
| C. | 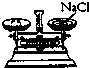 称取NaCI | D. | 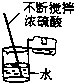 稀释浓硫酸 |
| 物 质 | 甲 | 乙 | 丙 | 丁 |
| 反应前质量/g | 1.7 | 1.3 | 5 | 7 |
| 反应后质量/g | 待测 | 12.3 | 1 | 0 |
| A. | 待测的值是1.7 | B. | 丙、丁在反应中的质量比为4:7 | ||
| C. | 物质甲可能是催化剂 | D. | 物质乙属于单质 |
| A. | 碳酸钠俗称纯碱,也叫苏打,可用于清洗厨房用具的油污 | |
| B. | 84消毒液在日常生活中使用广泛,溶液无色,有漂白作用,它的有效成分为Ca(ClO)2 | |
| C. | 青铜是我国使用最早的合金材料,目前世界上使用量最大的合金材料是铝合金 | |
| D. | 明矾[KAl(SO4)2•12H2O]溶于水会形成胶体,因此可用于自来水的消毒杀菌 |