题目内容
17.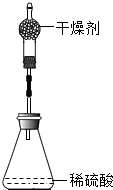 为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:
为测定锌铜合金中锌的含量,取该合金放入如图盛有稀硫酸的锥形瓶中.多次实验后,取平均值所得数据如表:| 反应前 | 充分反应后装置及反应剩余物质质量 | |
| 装置和足量的稀硫酸质量 | 锌铜合金质量 | |
| 342.10g | 16.00g | 357.70g |
(1)根据质量守恒定律求生成氢气的质量0.4g.
(2)该合金中锌的质量分数.
分析 铜不能和稀硫酸反应,锌和稀硫酸反应生成硫酸锌和氢气,反应前后的质量差即为反应生成氢气的质量,根据氢气的质量可以计算锌的质量,进一步可以计算锌的质量分数.
解答 解:(1)反应生成氢气的质量为:342.10g+16.00g-357.70g=0.4g,
故填:0.4g.
(2)设锌的质量为x,
Zn+H2SO4═ZnSO4+H2↑,
65 2
x 0.4g
$\frac{65}{x}$=$\frac{2}{0.4g}$,
x=13g,
该合金中锌的质量分数为:$\frac{13g}{16.00g}$×100%=81.25%,
答:该合金中锌的质量分数为81.25%.
点评 差量法在计算中的应用很广泛,解答的关键是要分析出物质的质量差与要求的未知数之间的关系,再根据具体的数据求解.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.正确的实验操作是科学探究成功的基础.下列操作中错误的是( )
| A. | 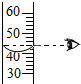 读出液体体积 | B. |  CO2的验满 | C. | 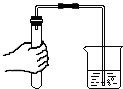 检查装置气密性 | D. | 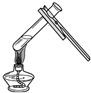 加热液体 |
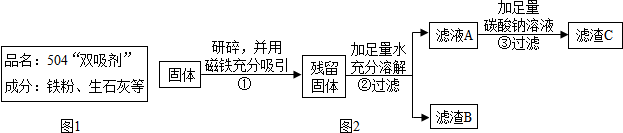
8.红枣中含有丰富的VC和糖类,常食能增强人体的免疫力,有补血养气安神等良好功效,红枣包装中常使用一种袋装防腐剂,品名为“504双吸剂”,其标签如图1所示.某化学兴趣小组对一包久置的“504双吸剂”固体样品产生浓厚的兴趣,设计实验进行探究.
【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
乙同学认为甲同学的实验并不能得出一定不含Fe2O3的结论,理由是氧化铁与稀盐酸反应生成的氯化铁又与铁粉反应生成氯化亚铁.
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
【反思与评价】甲、乙两同学经过讨论后,完善实验方案最终确定该久置固体的成分是Fe、Fe2O3、CaO、CaCO3.

【提出问题】久置固体的成分是什么?
【作出猜想】久置固体中可能含有Fe、Fe2O3、CaO、Ca(OH)2和CaCO3.
【查阅资料】铁与氯化铁溶液在常温下发生反应生成氯化亚铁.
【实验探究】甲同学的方案:
| 实验操作 | 实验现象 | 实验结论 |
取少量固体于试管中,滴 加足量的稀盐酸. | 固体逐渐消失,有大量无色气体产生,得到浅绿色溶液. | 固体中一定含有Fe, 一定不含Fe2O3. |
他设计如图2实验方案继续验证.
(1)步骤①样品用磁铁吸引前需经过研碎,其中研碎的目的是增大接触面积,使得铁粉能够充分吸引;
(2)②中固体溶解时放出大量热,由此可以判断固体中一定含有CaO.
(3)③中反应的化学方程式是Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
乙同学对滤渣B又进行探究.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量固体于试管中,滴加足量的稀盐酸,并将气体通入澄清石灰水 | 固体逐渐消失、有气泡产生、 澄清石灰水变浑浊、 溶液呈黄色. | 固体中一定含有CaCO3和Fe2O3. |
12.下列说法正确的是( )
| A. | 等质量的CO和CO2,CO和CO2中氧元素的质量比为11:14 | |
| B. | 等质量的Al和Mg分别与足量稀硫酸充分反应,生成H2的质量相等 | |
| C. | 等质量的NaHCO3和MgCO3分别与足量稀盐酸充分反应,生成CO2的质量不相等 | |
| D. | 等质量的质量分数均为4%氢氧化钠溶液与稀盐酸充分反应后,所得溶液显中性 |
2.下列叙述遵守质量守恒定律的是( )
| A. | 镁带在空气中燃烧后,生成物质量大于镁带的质量,此反应不遵守质量守恒定律 | |
| B. | 10g酒精和10g水混和,可得到20g酒精溶液 | |
| C. | 6g硫和6g氧气反应,可生成12g二氧化硫 | |
| D. | 12g碳和12g氧气反应,可得到24g二氧化碳 |
9.关于水的净化过程描述错误的是( )
| A. | 通过过滤装置除去可溶性杂质 | B. | 通入氯气杀菌消毒 | ||
| C. | 加入明矾使不溶性悬浮物凝聚 | D. | 通过活性炭吸附部分有害物质 |
6.下列各组物质在溶液中能大量共存且形成无色溶液的是( )
| A. | K2CO3 NaCl HCl | B. | CuSO4 H2SO4 NaNO3 | ||
| C. | BaCl2 AgNO3 Na2SO4 | D. | AlCl3 KNO3 Na2SO4 |
20.如表是某同学设计的物质鉴别方法,他设计的两种方法都正确的是( )
| 选项 | 需鉴别的物质 | 加试剂或方法 | |
| 方法1 | 方法2 | ||
| A | 稀盐酸、氯化钾溶液 | 无色酚酞、看颜色 | 加入铁粉、看气泡 |
| B | 生石灰、熟石灰 | 两种物质分别溶于水 | 向两种物质中分别加入稀盐酸 |
| C | 蒸馏水、酒精 | 分别点燃 | 品尝 |
| D | 厕所清洁剂、厨房洗涤剂 | 用pH试纸测定它们的pH | 分别加入少量石蕊试液 |
| A. | A | B. | B | C. | C | D. | D |