题目内容
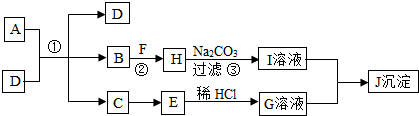
3.某实验小组的同学利用氢氧化钙溶液和稀盐酸进行酸碱中和反应的实验时,他们在向盛有氢氧化钙溶液的烧杯中滴加一定量的稀盐酸后,才发现忘记滴加了酸碱指示剂,此时,他们停止滴加稀盐酸,并对烧杯内溶液中所含溶质的成分进行探究.【提出猜想】
猜想一:溶质是CaCl2和Ca(OH)2
猜想二:溶质是CaCl2
猜想三:溶质是CaCl2和HCl.
【查阅资料】
①CaCl2溶液呈中性;
②有关的化学反应:
a.氢氧化钙溶液和稀盐酸进行中和反应的化学方程式为:Ca(OH)2+2HCl=CaCl2+2H2O
b.碳酸钠溶液和稀盐酸反应的化学方程式为:Na2CO3+2HCl=2NaCl+CO2↑+H2O
c.碳酸钠溶液和氯化钙溶液反应的化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl
【实验设计与验证】
(1)小猛同学设计用无色酚酞溶液验证“猜想一”是否成立.取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色.于是可以确定“猜想一”不成立(填“成立”或“不成立”),其理由是如果含有氢氧化钙,则酚酞试液变红色.
(2)小华同学设计用碳酸钠溶液验证“猜想二”和“猜想三”是否成立.取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入过量的碳酸钠溶液,观察到的现象是:先出现气泡,后有白色沉淀生成.于是可以确定猜想三成立.
【交流与反思】
经过同学们讨论和交流,发现只需用下列一种物质就能验证得出以上三种猜想中的哪一种猜想成立,请在下列物质的选项中选择出你认为合理的物质是B(填序号).
A.锌粒 B.紫色石蕊溶液 C.二氧化碳.
分析 【提出猜想】
氢氧化钙和稀盐酸反应生成氯化钙和水;
【实验设计与验证】
氢氧化钙溶液显碱性,能使酚酞试液变红色;
碳酸钠能和稀盐酸反应生成氯化钠、水和二氧化碳,能和氯化钙反应生成碳酸钙沉淀和氯化钠;
【交流与反思】
显碱性的溶液能使石蕊试液变蓝色,显酸性的溶液能使石蕊试液变红色,显中性的溶液不能使石蕊试液变色.
解答 解:【提出猜想】
溶质可能是CaCl2和Ca(OH)2,也可能是CaCl2,也可能是CaCl2和HCl.
故填:HCl.
【实验设计与验证】
(1)取少量上述实验中烧杯里的溶液于试管中,并向试管中滴加几滴无色酚酞溶液,振荡,观察到溶液不变色.于是可以确定“猜想一”不成立”,其理由是如果含有氢氧化钙,则酚酞试液变红色;
(2)取少量上述实验中烧杯里的溶液于试管中,并向试管中逐滴加入过量的碳酸钠溶液,先出现气泡,说明溶液中含有HCl,后有白色沉淀生成,说明溶液中含有氯化钙,于是可以确定猜想三成立.
故填:不成立;如果含有氢氧化钙,则酚酞试液变红色;白色沉淀;猜想三.
【交流与反思】
向上述实验中烧杯里的溶液中滴加适量的石蕊试液,如果溶液变红色,说明溶质是氯化钙和氢氧化钙;
如果溶液不变色,说明溶质是氯化钙;
如果溶液变红色,说明溶质是氯化钙和氯化氢.
故填:B.
点评 实验现象是物质之间相互作用的外在表现,因此要学会设计实验、观察实验、分析实验,为揭示物质之间相互作用的实质奠定基础.

练习册系列答案
相关题目
11.分析、类比和推理是化学学习中常用的思维方法.下列分析、类比和推理正确的是( )
| A. | 浓硫酸具有吸水性,所以浓盐酸也具有吸水性 | |
| B. | 酸雨的pH小于7,所以pH小于7的雨水一定是酸雨 | |
| C. | 离子是带电荷的微粒,所以带电荷的微粒一定是离子 | |
| D. | 组成CO和CO2的元素相同,但它们的分子构成不同,所以它们的化学性质不同 |
3.下列属于空气污染物的是( )
| A. | 一氧化碳 | B. | 二氧化碳 | C. | 氧气 | D. | 氮气 |
8.在密闭容器中有甲、乙、丙、丁四种物质,在一定条件下充分反应,测得反应前后各物质的质量分数如图所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 丙可能是单质 | |
| B. | 在该反应中丁一定没有参加化学反应 | |
| C. | 该反应是置换反应 | |
| D. | 参加反应的甲和乙的质量之和一定等于生成丙的质量 |
 请写出符合下列条件的化学方程式各一个:
请写出符合下列条件的化学方程式各一个: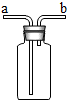 如图所示装置(不可倒置)有多种用途,下列叙述正确的是C
如图所示装置(不可倒置)有多种用途,下列叙述正确的是C