题目内容
18.下列数据是硝酸钾固体在不同温度时的溶解度.| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
分析 根据表格提供的数据进行分析,硝酸钾在60℃时的溶解度是110g,硝酸钾的溶解度随温度的升高而增大,据此解答.
解答 解:(1)硝酸钾在60℃时的溶解度是110g,即60℃时,l00g水中最多能溶解硝酸钾固体110g,故填:110;
(2)硝酸钾的溶解度随温度的升高而增大,当降低温度时,硝酸钾的饱和溶液会析出晶体,故填:会.
点评 本题考查了溶解度的知识,完成此题,可以依据题干提供的信息进行.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列实际应用中,利用中和反应原理的是( )
| A. | 用氢氧化钠溶液吸收二氧化硫 | B. | 用熟石灰处理泄漏的浓硫酸 | ||
| C. | 用小苏打治疗胃酸过多 | D. | 用生石灰作食品干燥剂 |
6.某烧碱样品有部分变质,为测定烧碱的纯度(假设样品中只有氢氧化钠和碳酸钠这两种成分,且碳酸钠是变质产生的),做了如下实验:取烧碱样品20g,分四次加入到36.5g一定浓度的稀盐酸中,数据如表所示
请根据提供的数据,回答下列问题:
(1)该实验产生了一种气体,该气体的化学式为CO2;表格中m的数值为49.3.
(2)请计算烧碱样品中烧碱的纯度.
| 实验次数 | 1 | 2 | 3 | 4 |
| 每次加入样品的质量/g | 5 | 5 | 5 | 5 |
| 反应后剩余物质的总质量/g | 40.4 | 44.3 | m | 54.3 |
(1)该实验产生了一种气体,该气体的化学式为CO2;表格中m的数值为49.3.
(2)请计算烧碱样品中烧碱的纯度.
13.下列实验操作不正确的是( )
| A. | 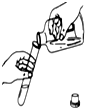 | B. |  | C. |  | D. | 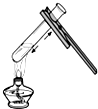 |
3.下列有关物质的除杂(括号内为杂质)或鉴别所用试剂和方法合理的是( )
| A. | MnO2(KCl)--加水溶解、过滤,蒸发结晶 | |
| B. | 铜粉(CuO)--在氧气流中灼烧 | |
| C. | 鉴别化肥NH4NO3和(NH4)2SO4---取样加熟石灰研磨 | |
| D. | 鉴别羊毛和涤纶----用点燃闻气味的方法 |
10.某化学研究小组的同学探究酸碱中和反应,选择的试剂是稀硫酸和氢氧化钠溶液,实验过程如下:
在一定量的M溶液中不断滴加N溶液,如甲图所示,并测定所得溶液的pH变化如乙图所示.

(1)M是①氢氧化钠溶液(NaOH),该反应的化学方程式②2NaOH+H2SO4═Na2SO4+2H2O
反应过程中测得溶液温度③升高(填“升高”.“降低”或“不变”).
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学测定溶液的pH,并探究其成分.
马明和古丽分别取其中一种溶液进行试验:马明向所取得溶液加入④CuSO4或CuCl2或Cu(NO3)2溶液,观察到有蓝色沉淀.
结论:是a溶液古丽向少量的里另一种溶液中滴加酚酞溶液,观察到⑤溶液呈无色或酚酞不变色.
为进一步确定该处的溶液成分,马明又设计并完成如下实验:
剩余一种为b溶液.通过实验,同学们知道了酸碱反应过程中pH的变化以及确定溶液成分的方法.
在一定量的M溶液中不断滴加N溶液,如甲图所示,并测定所得溶液的pH变化如乙图所示.

(1)M是①氢氧化钠溶液(NaOH),该反应的化学方程式②2NaOH+H2SO4═Na2SO4+2H2O
反应过程中测得溶液温度③升高(填“升高”.“降低”或“不变”).
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学测定溶液的pH,并探究其成分.
马明和古丽分别取其中一种溶液进行试验:马明向所取得溶液加入④CuSO4或CuCl2或Cu(NO3)2溶液,观察到有蓝色沉淀.
结论:是a溶液古丽向少量的里另一种溶液中滴加酚酞溶液,观察到⑤溶液呈无色或酚酞不变色.
为进一步确定该处的溶液成分,马明又设计并完成如下实验:
| 实验步骤 | 实验现象 | 结论 |
| ⑥取少量溶液,向其中滴加石蕊溶液 | ⑦溶液变红色 | 为C处溶液,并推至溶液中溶质有 ⑧H2SO4、Na2SO4(填化学式) |
16.下列实验合理的是( )
| A. | 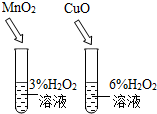 比较催化效果 | B. | 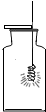 铁丝在纯氧中燃烧 | ||
| C. | 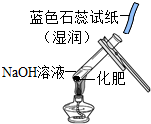 检验铵态氮肥 | D. | 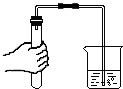 检查装置气密性 |
 如图为A、B、C三种物质的溶解度曲线.
如图为A、B、C三种物质的溶解度曲线.