题目内容
10.某化学研究小组的同学探究酸碱中和反应,选择的试剂是稀硫酸和氢氧化钠溶液,实验过程如下:在一定量的M溶液中不断滴加N溶液,如甲图所示,并测定所得溶液的pH变化如乙图所示.

(1)M是①氢氧化钠溶液(NaOH),该反应的化学方程式②2NaOH+H2SO4═Na2SO4+2H2O
反应过程中测得溶液温度③升高(填“升高”.“降低”或“不变”).
(2)反应过程中,老师取a、b、c三处反应后的溶液,打乱顺序后,请同学测定溶液的pH,并探究其成分.
马明和古丽分别取其中一种溶液进行试验:马明向所取得溶液加入④CuSO4或CuCl2或Cu(NO3)2溶液,观察到有蓝色沉淀.
结论:是a溶液古丽向少量的里另一种溶液中滴加酚酞溶液,观察到⑤溶液呈无色或酚酞不变色.
为进一步确定该处的溶液成分,马明又设计并完成如下实验:
| 实验步骤 | 实验现象 | 结论 |
| ⑥取少量溶液,向其中滴加石蕊溶液 | ⑦溶液变红色 | 为C处溶液,并推至溶液中溶质有 ⑧H2SO4、Na2SO4(填化学式) |
分析 (1)根据溶液pH的变化来分析;
(2)根据蓝色沉淀是氢氧化铜沉淀来分析;根据酸的性质来分析解答.
解答 解:(1)由图象可知,该溶液的pH由大变小,是向碱溶液中滴加酸溶液,故M是氢氧化钠溶液,二者反应生成硫酸钠和水,中和反应都会放出热量;故填:氢氧化钠溶液(NaOH);2NaOH+H2SO4═Na2SO4+2H2O;升高;
(2)能生成氢氧化铜蓝色沉淀,说明向碱性溶液中滴加了可溶性的铜盐溶液,故填:CuSO4 或CuCl2或Cu(NO3)2;
上述溶液显碱性,则另外两种溶液呈中性和酸性,均不能使无色酚酞试液变色;故填:溶液呈无色或酚酞不变色;
检验溶液呈中性还是酸性,可加入紫色的石蕊试液,若变红色,则为酸性,即C处的溶液,其中的溶质是硫酸钠和硫酸;
若不变色,则为中性溶液,即b处的溶液,其中的溶质只有硫酸钠.
故填:取少量溶液,向其中滴加石蕊溶液;溶液变红色;H2SO4、Na2SO4.
点评 本题难度不是很大,主要考查了中和反应及其应用,掌握溶液的酸碱性和溶液pH大小之间的关系、从数形结合的角度理解中和反应是正确解答本题的关键.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
18.下列数据是硝酸钾固体在不同温度时的溶解度.
(1)60℃时,l00g水中最多能溶解硝酸钾固体110g.
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
15.小明和他的同学在实验室发现上一次实验后忘记塞上瓶塞的氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体.他们怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
【讨论】小明同学认为,根据上述实验(1)(2)可推断,猜想②正确.而小张则认为猜想③也可能正确,理由是碳酸钠溶液也能使酚酞溶液变红.
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
7.反应2KMnO4+□X+3H2SO4=2MnSO4+K2SO4+5O2↑+8H2O,则下列说法正确的是( )
| A. | 该反应中,X前的化学计量系数为10 | |
| B. | X中所含元素的质量比为1:16 | |
| C. | 反应前后所有元素的化合价都变化了 | |
| D. | 该实验发生装置与实验室用高锰酸钾制氧气的发生装置相同 |
8.除去下列物质中所含的杂质,选用的试剂及方法均正确的是( )
| 选项 | 物质 | 杂质 | 试剂 | 方法 |
| A | CO2 | H2O(蒸汽) | NaOH固体 | 干燥 |
| B | KCl粉末 | KClO3 | 少量MnO2 | 加热 |
| C | NaNO3溶液 | NaCl | 过量AgNO3溶液 | 过滤 |
| D | FeCl2溶液 | CuCl2 | 过量Fe粉 | 过滤 |
| A. | A | B. | B | C. | C | D. | D |
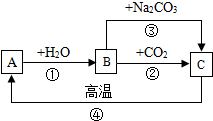 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):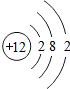 形成的离子用符号表示为Mg2+;
形成的离子用符号表示为Mg2+; 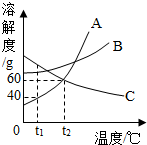 如图是 A、B、C三种物质的溶解度曲线.请回答:
如图是 A、B、C三种物质的溶解度曲线.请回答: