题目内容
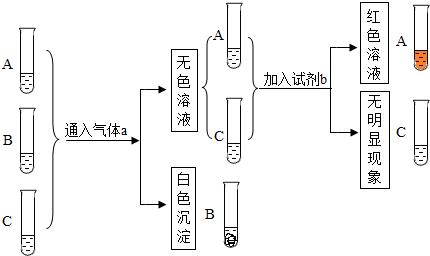
8. 如图为A、B、C三种物质的溶解度曲线.
如图为A、B、C三种物质的溶解度曲线.(1)0℃时,A的溶解度是20g.
(2)从A、B的混合物中分离A物质,一般采用降温结晶 的方法.
(3)t2℃时,A、B、C三种物质的溶解度大小关系是A=B>C;
将等质量的A、B、C三种物质的饱和溶液同时降温到t1℃,所得溶液中溶质质量分数最小的是C.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)根据A的溶解度曲线可知,在t1℃时,A的溶解度是20g;
(2)A物质的溶解度受温度影响变化较大,B物质的溶解度受温度影响变化较小,所以从A、B的混合物中分离A物质,一般采用降温结晶的方法;
(3)根据A、B、C三种物质的溶解度曲线可以看出,t2℃时,A、B、C三种物质的溶解度大小关系是:A=B>C;
t1℃时,B物质的溶解度比A物质的溶解度大,但是C物质的溶解度随温度的降低而增大,C物质t2℃比B物质t1℃时的溶解度小,所以所得溶液中溶质质量分数最小的是C.
故答案为:(1)20g;
(2)降温结晶;
(3)A=B>C;C.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
相关题目
18.为了除去物质中的杂质(括号内为杂质),如表方法正确的是( )
| 物 质 | 方法 |
| A.C(CuO) | 通入足量的CO后加热 |
| B.CaCl2溶液(HCl) | 加入过量Ca(OH)2溶液,使其充分反应 |
| C.CuSO4(H2SO4) | 加入过量CuO粉末,充分反应后过滤 |
| D.CO2(CO) | 点燃 |
| A. | A | B. | B | C. | C | D. | D |
19.化学兴趣小组查得资料:某品牌牙膏中的摩擦剂由碳酸钙、氢氧化铝等组成,牙膏中只有碳酸钙遇到盐酸时有气体产生.该小组对牙膏样品中碳酸钙的含量进行以下探究:
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.
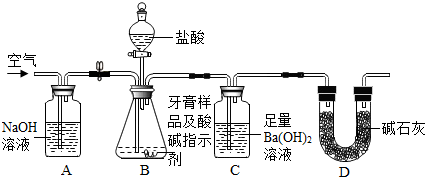
依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收
(2)下列各项措施中,不能提高测定准确度的是cd(填标号).
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(3)实验中准确称取8.00g样品四份,进行四次测定,每份测得BaCO3质量见表,则计算时所用BaCO3的质量为3.94g.
(4)某同学认为不必测定C中生成的BaCO3质量,只要测定装置C在吸收CO2前后的质量差,一样可以准确测定碳酸钙的质量分数.你是否同意此同学的观点否(填“是”或“否”),理由是B中的水蒸气、氯化氢气体等进入装置C中,导致测定二氧化碳的质量偏大,测定的碳酸钙的质量偏大,碳酸钙的质量分数偏高.
利用如图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定C中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数.

依据实验过程回答下列问题:
(1)实验过程中需持续缓缓通入空气,其作用除了可搅拌B、C中的反应物外,还有把生成的CO2气体全部排入C中,使之完全被Ba(OH)2溶液吸收
(2)下列各项措施中,不能提高测定准确度的是cd(填标号).
a.在加入盐酸之前,应排净装置内的CO2气体
b.滴加盐酸不宜过快
c.在A-B之间增添盛有浓硫酸的洗气装置
d.在B-C之间增添盛有饱和碳酸氢钠溶液的洗气装置
(3)实验中准确称取8.00g样品四份,进行四次测定,每份测得BaCO3质量见表,则计算时所用BaCO3的质量为3.94g.
| BaCO3的质量/g | |
| 第一份 | 3.94 |
| 第二份 | 1.10 |
| 第三份 | 3.93 |
| 第四份 | 3.95 |
16.生活中发生的下列变化中,不属于化学变化的是( )
| A. |  苹果腐烂 | B. |  榨取果汁 | C. |  面包发霉 | D. |  菜刀生锈 |
13.城市垃圾问题日益恶化,对环境以及人类健康构成严重威胁.下列说法不正确的是( )
| A. | 城市生活垃圾可以导致空气、水体和土壤污染 | |
| B. | 减少城市垃圾的最佳途径是焚烧城市垃圾 | |
| C. | 城市建筑工地的垃圾会增加空气中PM2.5的含量 | |
| D. | 城市内一次性塑料制品的使用加剧了城市垃圾的排放 |
18.下列数据是硝酸钾固体在不同温度时的溶解度.
(1)60℃时,l00g水中最多能溶解硝酸钾固体110g.
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
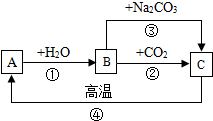 A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):
A、B、C是三种常见的含钙化合物.它们之间有如图所示的转化关系(部分产物略去):