题目内容
3.下列有关物质的除杂(括号内为杂质)或鉴别所用试剂和方法合理的是( )| A. | MnO2(KCl)--加水溶解、过滤,蒸发结晶 | |
| B. | 铜粉(CuO)--在氧气流中灼烧 | |
| C. | 鉴别化肥NH4NO3和(NH4)2SO4---取样加熟石灰研磨 | |
| D. | 鉴别羊毛和涤纶----用点燃闻气味的方法 |
分析 根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
铵态氮肥与碱性物质混合后能放出有刺激性气味的气体,羊毛的主要成分是蛋白质,蛋白质燃烧时能产生烧焦羽毛的气味,据此进行分析判断.
解答 解:A、氯化钾易溶于水,泥沙难溶于水,可采取加水溶解、过滤、洗涤、干燥的方法进行分离除杂,故选项所采取的方法错误.
B、铜粉在氧气流中灼烧生成氧化铜,反而会把原物质除去,不符合除杂原则,故选项所采取的方法错误.
C、NH4NO3和(NH4)2SO4均属于铵态氮肥,取样加熟石灰研磨,均产生有刺激性气味的气体,不能鉴别,故选项错误.
D、羊毛的主要成分是蛋白质,燃烧时有烧焦羽毛的气味,涤纶燃烧产生特殊气味,可用燃烧法区别羊毛和涤纶,故选项正确.
故选:D.
点评 物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目
13.城市垃圾问题日益恶化,对环境以及人类健康构成严重威胁.下列说法不正确的是( )
| A. | 城市生活垃圾可以导致空气、水体和土壤污染 | |
| B. | 减少城市垃圾的最佳途径是焚烧城市垃圾 | |
| C. | 城市建筑工地的垃圾会增加空气中PM2.5的含量 | |
| D. | 城市内一次性塑料制品的使用加剧了城市垃圾的排放 |
18.下列数据是硝酸钾固体在不同温度时的溶解度.
(1)60℃时,l00g水中最多能溶解硝酸钾固体110g.
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
| 温度/℃ | O | 20 | 40 | 60 | 80 |
| 溶解度/g | 13.3 | 31.6 | 63.9 | 110 | 169 |
(2)从上述表格信息可知,将80℃的硝酸钾饱和溶液降温到40℃,会(填“会”或“不会”)有硝酸钾晶体析出.
15.小明和他的同学在实验室发现上一次实验后忘记塞上瓶塞的氢氧化钠溶液的试剂瓶瓶口周围有一些白色固体.他们怀疑氢氧化钠溶液已经变质,于是进行了如下实验探究.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
【讨论】小明同学认为,根据上述实验(1)(2)可推断,猜想②正确.而小张则认为猜想③也可能正确,理由是碳酸钠溶液也能使酚酞溶液变红.
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
【提出问题】氢氧化钠溶液是否变质?
【提出猜想】①该氢氧化钠溶液没有变质; ②该氢氧化钠溶液部分变质;③该氢氧化钠溶液全部变质.
【实验验证】
| 操作 | 现象 | 结论 | 化学方程式 | |
| (1) | 取少量溶液于试管中,滴加无色酚酞溶液 | 无色酚酞变红 | 溶液显碱性 | |
| (2) | 取少量溶液于试管中,滴加稀盐酸 | 有气泡产生 | 溶液中存在碳酸根离子(或碳酸钠) | Na2CO3+2HCl═2NaCl+H2O+CO2↑ |
于是小王又设计了如下补充实验:
(1)取原溶液少量于试管中,逐滴加入BaCl2溶液至不再产生沉淀静置,分层.
(2)取上层清液,向其中加入CuSO4溶液,若有蓝色沉淀产生,则说明氢氧化钠溶液部分变质,化学方程式:CuSO4+2NaOH═Na2SO4+Cu(OH)2↓.反之则说明氢氧化钠溶液已经全部变质.
【反思】该氢氧化钠溶液变质的原因可能是(用化学方程式表示):2NaOH+CO2═Na2CO3+H2O.
12.某种H2和CO混合气体,其密度是O2的一半,则H2的体积的百分含量为( )
| A. | 40% | B. | 46% | C. | 50% | D. | 54% |
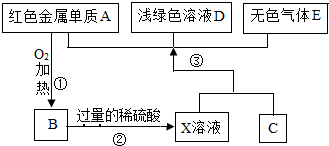 A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答:
A、B、C、D、E为初中化学常见的物质,其中A、C为金属单质,E为非金属单质,如图是它们之间的相互转化关系.请回答: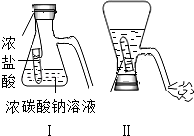 某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究.
某化学兴趣活动小组的同学学习“灭火器原理”后,设计了如图所示实验,并对反应后锥形瓶中残留废液进行探究.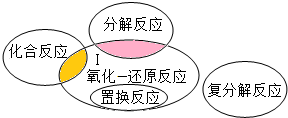 在化学反应前后,物质所含元素化合价发生变化的应是氧化-还原反应,它与初中所学的化学反应基本类型关系如图所示下:
在化学反应前后,物质所含元素化合价发生变化的应是氧化-还原反应,它与初中所学的化学反应基本类型关系如图所示下: