题目内容
9.石膏(CaSO4•2H2O)是一种用途广泛的工业材料和建筑材料,工业上用含SO2的烟气制备石膏的简要流程图如下:(CaSO4难溶于水)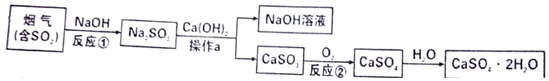
(1)在反应①时,常将NaOH喷成雾状的原因是增大与二氧化硫的接触面积,提高吸收或者反应的速率.
(2)操作a的名称是过滤,在实验室里进行该操作,玻璃棒的作用是引流.
(3)CaSO3属于盐(填“酸”或“碱”或“盐”),反应②的化学方程式是2CaSO3+O2=2CaSO4.
(4)生产流程中生成的氢氧化钠溶液可循环利用,节约成本.
分析 根据给出的转化关系对应的过程分析每个对应的问题,或者直接分析每个问题,从给出的信息中找对应的信息.
解答 解:(1)由于接触面积越大,反应速率越大或者吸收效率越高,所以在反应①时,常将NaOH喷成雾状.这样增大与二氧化硫的接触面积,提高吸收或者反应的速率.
(2)操作a是将难溶性物质亚硫酸钙和可溶性物质氢氧化钠分离的,所以是过滤.在实验室里进行过滤操作时,玻璃棒的作用是 引流.
(3)CaSO3,是金属离子和酸根离子形成的化合物,为盐.反应②中反应物为亚硫酸钙和氧气,生成物为硫酸钙,所以对应的化学方程式是 2CaSO3+O2=2CaSO4.
(4)由于反应过程需要用到氢氧化钠溶液,而中间过程也会生成氢氧化钠,所以在过程可以循环使用氢氧化钠溶液,以便节约成本减少环境污染.
故答案为:
(1)增大与二氧化硫的接触面积,提高吸收或者反应的速率.
(2)过滤;引流.
(3)盐; 2CaSO3+O2=2CaSO4.
(4)氢氧化钠溶液.
点评 读图,从中获得解答题目所需的信息,所以在解答题目时先看解答的问题是什么,然后带着问题去读给出的图进而去寻找解答有用的信息,这样提高了信息扑捉的有效性.解答的问题实际上与复杂的转化图相比,其实很简单很基础,或者可以说转化图提供的是情境,考查基本知识.

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
19.生活中的下列现象不能说明气体溶解度随温度升高而减小的是( )
| A. | 打开啤酒瓶盖有大量泡沫逸出 | B. | 烧开水时沸腾前有气泡逸出 | ||
| C. | 喝下汽水感到有气味冲到鼻腔 | D. | 夏季黄昏池塘里的鱼常浮出水面 |
17.有一包白色粉末,可能由氯化钠、硫酸钠、硫酸铜、碳酸钠、碳酸钙中的一种或几种组成,为确定其组成,进行如下实验:
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A;
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为20g;
③在20g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出;
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀;
根据上述实验现象判断,下列说法正确的是( )
①称取一定质量的该白色粉末加足量水溶解,得无色溶液A;
②在无色溶液A中加入过量氯化钡溶液,充分反应后过滤,分别得无色溶液B和白色沉淀C;将白色沉淀C洗涤,烘干后称得质量为20g;
③在20g白色沉淀C中加入足量的稀硝酸,沉淀部分消失,并有气泡冒出;
④在无色溶液B中滴加硝酸银溶液和稀硝酸,产生白色沉淀;
根据上述实验现象判断,下列说法正确的是( )
| A. | 白色粉末中一定含有氯化钠 | |
| B. | 无色溶液B中只含有一种溶质 | |
| C. | 步骤③生成的气体质量可能是4.4g | |
| D. | 白色粉末中不含碳酸钙、硫酸钠、硫酸铜 |
4.青少年正处在生长发育期,营养必须要均衡,如图中的食品中,富含糖类的是( )
| A. |  大米 | B. |  青菜 | C. |  豆类 | D. |  虾皮 |
1.下列选项中不属于化学研究领域的是( )
| A. | 研发氢能源 | B. | 编写电脑程序 | C. | 合成新材料 | D. | 冶炼金属 |
8.下列生活中各物质属于纯净物的是( )
| A. | 食品袋内防腐的氮气 | B. | 矿泉水 | ||
| C. | 可乐炊料 | D. | 加热高锰酸钾后的残留物 |

 化学兴趣小组的同学欲测定一瓶稀盐酸的溶质质量分数,具体步骤如下:
化学兴趣小组的同学欲测定一瓶稀盐酸的溶质质量分数,具体步骤如下: