题目内容
 请根据你学习的有关溶液的知识,回答下列问题:
请根据你学习的有关溶液的知识,回答下列问题:(1)溶液所具有的典型特征是
(2)下表列出的是从探究实验中获取的部分数据,请你根据这些数据,在如图的坐标图中绘制A、B两物质的溶解度 曲线(图中注明A、B).
| 温度/℃ | 0 | 20 | 40 | 60 | |
| 溶解度/g | A物质 | 30 | 35 | 45 | 50 |
| B物质 | 25 | 35 | 55 | 90 | |
(4)在20℃时,向100g水中加入40gA物质充分溶解后,形成的A物质溶液的溶质质量分数是
考点:溶液的概念、组成及其特点,固体溶解度曲线及其作用,晶体和结晶的概念与现象,有关溶质质量分数的简单计算
专题:溶液、浊液与溶解度
分析:(1)从溶液的特征是均一的、稳定的混合物去分析解答;
(2)从溶解度曲线是固体物质的溶解度随温度变化的曲线,物质的溶解度与温度是一一对应的关系去分析解答;
(3)看出A、B两种物质的溶解度都随温度的升高而增大,当温度降低时溶解度变小,晶体析出去分析解答;
(4)从溶质的质量分数的计算公式去分析解答.
(2)从溶解度曲线是固体物质的溶解度随温度变化的曲线,物质的溶解度与温度是一一对应的关系去分析解答;
(3)看出A、B两种物质的溶解度都随温度的升高而增大,当温度降低时溶解度变小,晶体析出去分析解答;
(4)从溶质的质量分数的计算公式去分析解答.
解答:解:(1)溶液的特征是均一的、稳定的混合物;故答案为:是均一的、稳定的混合物;
(2)溶解度曲线是固体物质的溶解度随温度变化的曲线,物质的溶解度与温度是一一对应的关系,从图中横坐标中分别找到0℃、20℃、40℃、60℃时A、B两种物质对应的溶解度,然后把每个点用平滑的曲线连接起来就可以了;答案如右图: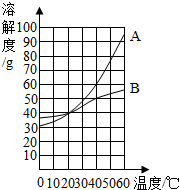 ;
;
(3)由上图可以看出A、B两种物质的溶解度都随温度的升高而增大,当温度降低时溶解度变小,以100g水形成B的饱和溶液由20℃降温到10℃为例,析出晶体的质量为:35g-15g(由图中可找出10℃时B的溶解度)=20g;由于A溶解度曲线受温度的影响不如B,所以B析出晶体的质量比A大,故答案为:小于;
(4)在20℃时,由表中可知此时A物质的溶解度为35g,加入40gA物质充分溶解后,由于最多能溶解35g,D故形成的A物质溶液的溶质质量分数为:
×100%=25.9%;故答案为:25.9%.
(2)溶解度曲线是固体物质的溶解度随温度变化的曲线,物质的溶解度与温度是一一对应的关系,从图中横坐标中分别找到0℃、20℃、40℃、60℃时A、B两种物质对应的溶解度,然后把每个点用平滑的曲线连接起来就可以了;答案如右图:
 ;
;(3)由上图可以看出A、B两种物质的溶解度都随温度的升高而增大,当温度降低时溶解度变小,以100g水形成B的饱和溶液由20℃降温到10℃为例,析出晶体的质量为:35g-15g(由图中可找出10℃时B的溶解度)=20g;由于A溶解度曲线受温度的影响不如B,所以B析出晶体的质量比A大,故答案为:小于;
(4)在20℃时,由表中可知此时A物质的溶解度为35g,加入40gA物质充分溶解后,由于最多能溶解35g,D故形成的A物质溶液的溶质质量分数为:
| 35g |
| 100g+35g |
点评:计算溶质质量分数时,一定要注意物质的溶解度,看溶质是否有剩余.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
能源问题是困扰当今世界难题之一,下列有关能源的叙述中不正确的是( )
| A、乙醇汽油中添加的乙醇属于可再生能源 |
| B、人类通过化石燃料获得能量的过程是物理变化 |
| C、将煤炭资源气化应用可有效降低缓解雾霾天气 |
| D、我国南海“可燃冰”,可能成为替代化石燃料的新能源 |
下列操作中,能区别空气、氧气2瓶气体的是( )
| A、加水溶解 |
| B、闻气体的气味 |
| C、加入澄清石灰水 |
| D、插入带火星的木条 |
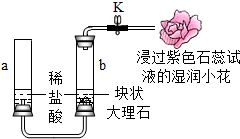 某实验小组用如图装置研究CO2的性质.提示:
某实验小组用如图装置研究CO2的性质.提示:

 甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中正确的是
甲、乙两种固体物质的溶解度曲线如图所示.下列有关叙述中正确的是