题目内容
3.实验室中含有盐酸的废水倒入下水道会造成铸铁管道腐蚀,下列对废水处理措施可行的是( )| A. | 加水稀释 | B. | 加入硼酸 | C. | 加入铜粉 | D. | 加入熟石灰 |
分析 根据盐酸具有酸性,直接倒入下水道,会造成管道腐蚀,所以需处理成中性后再排放解答.
解答 解:
A、加水稀释,酸性减弱,不能消除酸,故错误;
B、加入硼酸,酸性增强,不能消除酸,故错误;
C、加入铜粉,铜在氢的后面,与酸不反应,不能消除酸,故错误;
D、加入熟石灰,加碱性物质氢氧化钙处理成中性在排放,该反应的化学方程式为:Ca(OH)2+2HCl═CaCl2+2H2O,可以防止铸铁管道腐蚀,故正确.
答案:D
点评 本题难度不大,掌握酸的化学性质是正确解答本题的关键.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
7.”国富民强”,我国制碱工业的先驱-侯德榜,在积贫积弱的旧中国与诺贝尔奖无缘.“侯氏制碱”制得的是( )
| A. | NaOH | B. | NaHCO3 | C. | Na2CO3 | D. | Ca(OH)2 |
18.五氧化二钒(V2O5)可用于冶炼钒钢,其中钒(V)元素的化合价是( )
| A. | +5 | B. | +3 | C. | +2 | D. | +1 |
8.向FeSO4、CuSO4溶液中加入一定量的锌粉充分反应,下列情况中可能出现的是( )
①溶液中有Zn2+、Fe2+、Cu2+,不溶物为Cu
②溶液中有Zn2+、Fe2+,不溶物为Zn
③溶液中有Zn2+、Fe2+、,不溶物为Fe、Cu
④溶液中有Fe2+、Cu2+,不溶物为Zn、Cu.
①溶液中有Zn2+、Fe2+、Cu2+,不溶物为Cu
②溶液中有Zn2+、Fe2+,不溶物为Zn
③溶液中有Zn2+、Fe2+、,不溶物为Fe、Cu
④溶液中有Fe2+、Cu2+,不溶物为Zn、Cu.
| A. | ①③ | B. | ③④ | C. | ①② | D. | ②③ |
12.如图所示实验操作符合规范的是( )
| A. | 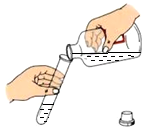 倾倒液体 | B. | 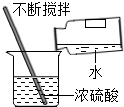 浓硫酸的稀释 | ||
| C. | 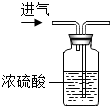 干燥氧气 | D. | 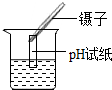 测定某溶液的pH值 |

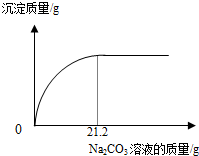 兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
 ,硫原子在化学反应中易得到(填“得到”或“失去”)电子,由钠元素和硫元素组成的化合物硫化钠的化学式为Na2S
,硫原子在化学反应中易得到(填“得到”或“失去”)电子,由钠元素和硫元素组成的化合物硫化钠的化学式为Na2S