题目内容
6.海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等.综合利用海水制备金属镁的流程如图表示:
(1)贝壳的主要成分的化学式是CaCO3.
(2)操作a的名称是过滤,在实验室中进行此项操作,需要的玻璃仪器有烧杯、玻璃棒、漏斗.
(3)写出第②步的反应现象放出大量的热
(4)写出第③步中和反应的化学方程式:Mg(OH)2+2HCl=MgCl2+2H2O.
(5)上述①、②、③、④四步反应未涉及的基本反应类型是置换反应.
分析 (1)碳酸钙以多种物质形式在自然界中存在,贝壳、蛋壳、石灰石等主要成分都是碳酸钙;
(2)过滤是分离固液混合物的常用的操作方法,该操作后可得到溶液和固体;根据操作需要,判断完成该操作需要的玻璃仪器;
(3)根据氧化钙与水反应放热进行分析;
(4)根据氢氧化镁与盐酸反应生成氯化镁和水进行分析;
(5)根据化学反应的类型分析解答即可.
解答 解:(1)贝壳主要成分为碳酸钙,其化学式是CaCO3;
(2)根据操作a完成后得到溶液和氢氧化镁的固体沉淀物,可判断操作a为过滤操作;该操作过程中除使用烧杯、玻璃棒外,还需要使用玻璃仪器漏斗;
(3)氧化钙与水反应放热,使溶液温度升高;
(4)第③步反应为氢氧化镁与盐酸反应生成氯化镁和水,化学方程式为:Mg(OH)2+2HCl═MgCl2+2H2O;
(5)①是碳酸钙高温煅烧生成氧化钙和二氧化碳,属于分解反应;②是氧化钙和水反应生成氢氧化钙,属于化合反应;③是氢氧化镁能和盐酸反应生成氯化镁和水,属于复分解反应,而④是电解MgCl2生成金属镁和氯气,属于分解反应,所以没有涉及的基本反应类型是置换反应.
故答案为:(1)CaCO3;(2)过滤;漏斗;(3)放出大量的热;(4)Mg(OH)2+2HCl=MgCl2+2H2O;(5)置换反应.
点评 利用流程图分析利用海水制备金属镁的流程,明确流程中所进行的操作和发生的反应,这是解决问题的基本方法.

练习册系列答案
 尖子生新课堂课时作业系列答案
尖子生新课堂课时作业系列答案 英才计划同步课时高效训练系列答案
英才计划同步课时高效训练系列答案
相关题目
16.现有化学反应2A+B═C+3D,下列说法正确的是( )
| A. | A和B的质量比一定等于C和D的质量比 | |
| B. | A和B相对分子质量比为44:36,则C和D的相对发展质量的比也是44:36 | |
| C. | 若A和B各取2g使其反应,则C和D的质量总和一定等于4g | |
| D. | A和B各取2g恰好完全反应,则C和D的质量总和一定等于4g |
3.实验室中含有盐酸的废水倒入下水道会造成铸铁管道腐蚀,下列对废水处理措施可行的是( )
| A. | 加水稀释 | B. | 加入硼酸 | C. | 加入铜粉 | D. | 加入熟石灰 |
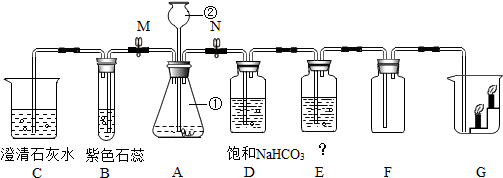
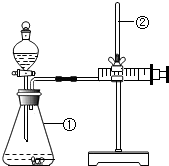 气体制取是初中毕业生应该掌握的一项操作技能,试根据下列装置图回答有关问题.
气体制取是初中毕业生应该掌握的一项操作技能,试根据下列装置图回答有关问题.