题目内容
11. 兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.
兴趣小组欲测定某未知浓度Ba(OH)2溶液的溶质质量分数,请你和他们一起完成实验并回答有关问题.(1)配制30g 10%的Na2CO3溶液.量取蒸馏水所需量筒的规格是50(从10、50、100中选择)mL.最后将碳酸钠溶液转移到试剂瓶中,贴上标签备用,在标签上可以不必注明的是A(填序号).
A.30g B.10% C.Na2CO3溶液
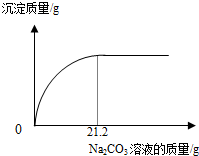
(2)测定未知浓度Ba(OH)2溶液的溶质质量分数.取50g Ba(OH)2溶液,逐滴滴加上述Na2CO3溶液的过程中,测得产生沉淀与加入Na2CO3溶液的质量关系如图所示.
①恰好完全反应时,消耗Na2CO3溶液的质量为21.2 g.
②请通过计算确定Ba(OH)2溶液的溶质质量分数.
已知:Ba(OH)2+Na2CO3=BaCO3↓+2NaOH.
分析 (1)根据配制一定溶质质量分数的溶液的方法来回答;根据量筒的选用原则解答;根据标签上的内容书写规范来回答;
(2)①根据图象分析解答;
②根据Na2CO3的质量,利用化学方程式,求出Ba(OH)2的质量,从而求出Ba(OH)2溶液的溶质质量分数.
解答 解:(1)配制一定物质的量浓度的溶液的步骤:计算、称取、量取、溶解、转移;配制30g 10%的Na2CO3溶液需水的质量为:30g×(1-10%)=27g,水的体积为27mL,量取水时应选用规格为50mL的量筒;标签上的内容应写上物质名称和溶质质量分数,因此在标签上可以不必注明的是溶液质量30g,故选:A;
(2)①通过分析图象可知,恰好完全反应时,消耗Na2CO3溶液的质量为21.2g;
②设Ba(OH)2的质量为x,Na2CO3溶液的质量中溶质的质量为:21.2g×10%=2.12g
Na2CO3+Ba(OH)2═BaCO3↓+2NaOH
106 171
2.12g x
$\frac{106}{21.2g}$=$\frac{171}{x}$
x=3.42g
氢氧化钡溶液溶质质量分数为:$\frac{3.42g}{50g}$×100%=6.84%.
故答案为:(1)溶解,50,A;
(2)①21.2;
②氢氧化钡溶液中溶质质量分数6.84%.
点评 本题考查学生配制一定物质的量浓度的溶液的步骤与及实验操作知识,可以根据教材知识来回答,难度不大.

练习册系列答案
 王后雄学案教材完全解读系列答案
王后雄学案教材完全解读系列答案
相关题目
16.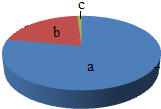 如图是空气成分示意图(按体积计算),其中“b”代表的是( )
如图是空气成分示意图(按体积计算),其中“b”代表的是( )
 如图是空气成分示意图(按体积计算),其中“b”代表的是( )
如图是空气成分示意图(按体积计算),其中“b”代表的是( )| A. | 氧气 | B. | 氮气 | C. | 二氧化碳 | D. | 稀有气体 |
3.实验室中含有盐酸的废水倒入下水道会造成铸铁管道腐蚀,下列对废水处理措施可行的是( )
| A. | 加水稀释 | B. | 加入硼酸 | C. | 加入铜粉 | D. | 加入熟石灰 |
1.乙酸乙酯(C4H8O2)常用作食品、饮料的调香剂.下列有关乙酸乙酯的叙述正确的是( )
| A. | 由14个原子构成 | B. | 氧元素的质量分数最小 | ||
| C. | 是由多种元素组成的混合物 | D. | 氢、氧元素质量比为1:4 |