题目内容
1.如图A是实验室制取二氧化碳并检验其性质的实验装置图,请你回答:
(1)a仪器的名称为长颈漏斗.
(2)写出实验室制取二氧化碳的化学方程式CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)小雨同学按图A方式将导管伸入试管中,溶液未出现浑浊现象,你认为可能的原因是装置的气密性不好或使用盐酸浓度过大(答出一条即可).
(4)为了制取方便,小林同学设计了如图B、C、D三种改进装置,你认为能起到“控制反应的发生和停止”效果的是CD(填序号).
分析 (1)熟记仪器的名称;
(2)根据实验室制取二氧化碳是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳进行分析.
(3)根据实验中的注意事项来分析;
(4)“随开随制,随关随停”,考虑反应物与反应物是否随时分开.
解答 解:(1)a是长颈漏斗,故填:长颈漏斗;
(2)实验室制取二氧化碳是碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,化学方程式为:CaCO3+2HCl=CaCl2+H2O+CO2↑.故答案为:CaCO3+2HCl=CaCl2+H2O+CO2↑.
(3)结果他没有看到澄清的石灰水变浑浊,则所可能装置漏气;若反应物盐酸过浓,使制的二氧化碳中含有HCl气体;故答:装置的气密性不好或使用盐酸浓度过大.
(4)为了制取方便,小聪同学设计了如图B、C、D三种改进装置,能起到“随开随制,随关随停”效果的是 CD.故填:CD.
点评 解答本题,首先要了解启普发生器的原理:将生成的气体密封后,能使密封空间内的压强增大,从而将液体压离固体,从而实现固液分离的目的.

练习册系列答案
相关题目
6.下列基本反应类型中,一定属于氧化还原反应的是( )
| A. | 复分解反应 | B. | 置换反应 | C. | 分解反应 | D. | 化合反应 |
13.某氯化钠溶液中含有少量的氯化钡和氢氧化钠溶液杂质,它们的质量比为13:10.欲将两种杂质同时除去,得到纯净的氯化钠溶液,可选用的试剂组合是( )
| A. | 盐酸和硫酸溶液,其溶质的质量比为146:98 | |
| B. | 盐酸和硫酸钠溶液,其质量比为73:71 | |
| C. | 硫酸和硫酸钠溶液,其质量比为98:71 | |
| D. | 硫酸和硫酸镁溶液,其溶质的质量比为49:60 |
10.下列属于纯净物的是( )
| A. | 肥皂水 | B. | 不锈钢 | C. | 金刚石 | D. | 食用醋 |
 A~G是初中常见的7种物质,它们有如图所示的转化关系.已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.
A~G是初中常见的7种物质,它们有如图所示的转化关系.已知A、C是无色液体,B、F、G是无色气体,其中大量排放F会引起温室效应,D是黑色固体,E在纯净的B中燃烧发出明亮的蓝紫色火焰.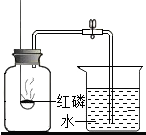 如图是实验室测定空气中氧气的体积分数的实验装置
如图是实验室测定空气中氧气的体积分数的实验装置 根据如图的原子结构示意图回答下列问题.
根据如图的原子结构示意图回答下列问题.