题目内容
2.SO2是形成酸雨的主要污染物之一,目前较为有效的处理方法是在高空喷洒一种粉末状的物质X,脱硫效果可以达到85%,化学反应方程式为2X+2SO2+O2=2CaSO4+2CO2↑,由此可知X的化学式是( )| A. | CaO | B. | CaS | C. | CaCO3 | D. | Ca(OH)2 |
分析 由质量守恒定律:反应前后,原子种类、数目均不变,据此由反应的化学方程式推断反应物X的化学式.
解答 解:由质量守恒定律:反应前后,原子种类、数目均不变,由反应的化学方程式2X+2SO2+O2=2CaSO4+2CO2↑,反应前钙、硫、碳、氧原子个数分别为0、2、0、6,反应后的生成物中钙、硫、碳、氧原子个数分别为2、2、2、12、根据反应前后原子种类、数目不变,则2X分子中含有2个钙原子、2个碳原子和6个氧原子,则每个X分子由1个钙原子、1个碳原子和3个氧原子构成,则物质X的化学式为CaCO3.
故选:C.
点评 本题难度不大,掌握利用化学反应前后原子守恒来确定物质的化学式的方法是正确解答此类题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
12.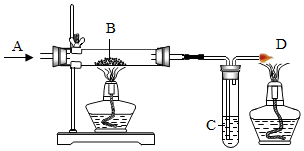 小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
(1)根据要求完成下表填写:
(2)实验Ⅰ通过B处的现象已能确定有铜这种产物,还需要在B与C之间加装一个装有无水硫酸铜(填药品名称)的干燥管,就能确定另一产物是水.
(3)实验Ⅱ、Ⅲ的D处导管尖嘴口需用酒精灯点燃的目的是把一氧化碳转化成二氧化碳,防止污染环境.
 小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.
小陈利用如图所示装置进行气体性质的探究实验.A处通入无色气体(可能是H2或CO);B处玻璃管中盛放黑色粉末CuO,C处试管中盛放澄清石灰水溶液.(1)根据要求完成下表填写:
| 序号 | 探究实验 | 简答 |
| Ⅰ | 若为H2与CuO的反应 | B处玻璃管观察到现象:出现水珠. |
| Ⅱ | 若为CO与CuO的反应 | B处反应的化学方程式:CuO+CO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2, 发生氧化反应的物质是:CO. |
| Ⅲ | 若为CO2与C 的反应 (B处换成酒精喷灯加热) | B处的黑色粉末逐渐减少,最后消失, D处观察到有蓝色的火焰. |
(3)实验Ⅱ、Ⅲ的D处导管尖嘴口需用酒精灯点燃的目的是把一氧化碳转化成二氧化碳,防止污染环境.
13.由A、B两种元素组成的物质中,A、B元素的相对原子质量比7:2,A、B元素的质量比7:3,则该物质是( )
| A. | A2B | B. | A2B3 | C. | AB2 | D. | A3B2 |
7.为了除去粗盐中的Ca2+、Mg2+、SO42-及泥砂,可将粗盐溶于水,然后进行下列五项操作①过滤;②加过量NaOH溶液;③加适量盐酸;④加过量Na2CO3溶液;⑤加过量BaCl2溶液.下列操作顺序中最合适的是( )
| A. | ①④②⑤③ | B. | ④①②⑤③ | C. | ②⑤④①③ | D. | ⑤②④③① |
11.在通常情况下,鉴别氢气和氧气不可以利用的方法是( )
| A. | 分别用带火星的木条伸入气体中 | B. | 观察颜色、状态、闻气味 | ||
| C. | 分别用吹肥皂泡的方法 | D. | 通电电解后利用电极来判断 |
12.小明在家准备腌制盐鸭蛋,他从网上查得一份资料:
饱和食盐水腌制法
水和盐的用量按鸭蛋的多少来定.腌制时先将食盐溶于烧开的水中,待盐水冷却至室温(20℃)时达到饱和状态.将冷却后的饱和食盐水倒入坛中,把洗净晾干的鸭蛋,逐个放进盐水中,密封坛口,25天左右即可开坛取蛋煮食.于是小明取2千克水于锅中,准备烧开后加入食盐,为避免浪费,请你根据下表氯化钠不同温度下的溶解度计算:
(1)小明至少要放720克食盐才能得到室温下的饱和溶液.
(2)求此时的溶液中食盐的质量分数.
(3)若要将质量分数为20%的食盐水45克,稀释成0.9%的食盐水,需加水多少克?
饱和食盐水腌制法
水和盐的用量按鸭蛋的多少来定.腌制时先将食盐溶于烧开的水中,待盐水冷却至室温(20℃)时达到饱和状态.将冷却后的饱和食盐水倒入坛中,把洗净晾干的鸭蛋,逐个放进盐水中,密封坛口,25天左右即可开坛取蛋煮食.于是小明取2千克水于锅中,准备烧开后加入食盐,为避免浪费,请你根据下表氯化钠不同温度下的溶解度计算:
| 温度/℃ | 0 | 10 | 20 | 40 | 60 | 80 | 100 |
| 氯化钠/克 | 35.7 | 35.8 | 36 | 36.6 | 37.3 | 38.4 | 39.8 |
(2)求此时的溶液中食盐的质量分数.
(3)若要将质量分数为20%的食盐水45克,稀释成0.9%的食盐水,需加水多少克?
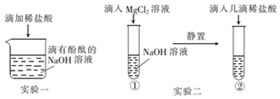 实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答:
实验小组在探究“酸与碱能否发生反应”时,进行了如图所示实验.请根据实验回答: