题目内容
13.由A、B两种元素组成的物质中,A、B元素的相对原子质量比7:2,A、B元素的质量比7:3,则该物质是( )| A. | A2B | B. | A2B3 | C. | AB2 | D. | A3B2 |
分析 根据化合物中各元素质量比=各原子的相对原子质量×原子个数之比,进行分析解答.
解答 解:由A、B两种元素组成的物质中,A、B元素的相对原子质量比7:2,A、B元素的质量比7:3,则该物质的分子中A、B原子的质量比为$\frac{7}{7}$:$\frac{3}{2}$=2:3,则该物质是A2B3.
故选:B.
点评 本题难度不大,灵活运用化学式的有关计算(相对分子质量、质量比、元素的质量分数、化合物中某元素的质量等)是正确解答此类题的关键.

练习册系列答案
相关题目
8.下列有关物态变化的叙述正确的是( )
| A. |  冰熔化过程中冰水混合物温度高于0℃ | |
| B. |  冷冻室取出的冰棍,外表的“霜”是由空气中水蒸气凝华而成 | |
| C. |  通常采用降温的方法将石油气液化储存在钢罐内 | |
| D. |  舞台上的云雾是干冰升华成的二氧化碳气体 |
18.量取47毫升的水,应选用下列( )
| A. | 100毫升的量筒 | B. | 100毫升的量筒和滴管 | ||
| C. | 50毫升的量筒和滴管 | D. | 50毫升的量筒 |
2.SO2是形成酸雨的主要污染物之一,目前较为有效的处理方法是在高空喷洒一种粉末状的物质X,脱硫效果可以达到85%,化学反应方程式为2X+2SO2+O2=2CaSO4+2CO2↑,由此可知X的化学式是( )
| A. | CaO | B. | CaS | C. | CaCO3 | D. | Ca(OH)2 |
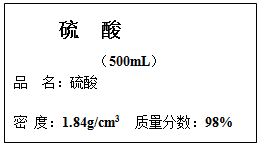 如图是学校实验室中硫酸试剂的标签,请阅读后计算下列试题.
如图是学校实验室中硫酸试剂的标签,请阅读后计算下列试题.