题目内容
15.实验室利用如图实验装置进行有关化学实验,请回答下列问题:
(1)某同学选择A装置用高锰酸钾制取氧气,反应的化学方程式为:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,为防止高锰酸钾粉末进入导管,应采取的措施是加热时试管口要放一团棉花,.
(2)实验室制取二氧化碳的化学方程式是CaCO3+2HCl═CaCl2+H2O+CO2↑,用装置C收集二氧化碳,验满的方法是将燃着的木条伸到a管处,如果熄灭,则证明已满.
(3)用上述制取二氧化碳实验后的固液残留物进行过滤、蒸发的操作训练.
①对固液残留物进行过滤,应选择图中D(填标号)装置,该装置缺少的仪器是玻璃棒,该仪器的作用是引流;
②取上述少量滤液进行蒸发,蒸发时玻璃棒不断搅拌的目的是液体受热均匀,防止液体飞溅,析出的固体中一定含有的物质是氯化钙(写化学式).
分析 (1)加热高锰酸钾制取氧气属于固体加热型,据反应原理书写方程式,加热时试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管;
(2)实验室制取二氧化碳用大理石和稀盐酸常温反应制取,据反应原理书写方程式;
(3)根据固液分离可以用过滤的方法,根据蒸发实验中玻璃棒的作用是搅拌,防止液体受热不均,溅出伤人.
解答 解:
(1)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,故反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,加热时试管口要放一团棉花,防止加热时高锰酸钾粉末进入导管;
(2)实验室大理石的主要成分碳酸钙和盐酸反应生成氯化钙、水和二氧化碳,反应方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑;用装置C收集二氧化碳,验满的方法是将燃着的木条伸到a管处,如果熄灭,则证明已满;
(3)①固液分离可以用过滤的方法,过滤时玻璃棒的作用是引流;
②蒸发实验中要用玻璃棒不断搅拌,为的是使液体受热均匀,防止液体飞溅.析出的固体中一定含有的物质是氯化钙.
故答案为:
(1)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;在试管口放一团棉花;
(2)CaCO3+2HCl═CaCl2+H2O+CO2↑;
(3)①D;玻璃棒;引流;②液体受热均匀,防止液体飞溅;氯化钙.
点评 据反应物状态和反应条件选择发生装置,据气体的密度和溶解性选择收集装置,并了解制取氧气、二氧化碳的反应原理,检验方法,注意事项等知识,才能结合题意灵活解答.

练习册系列答案
 举一反三单元同步过关卷系列答案
举一反三单元同步过关卷系列答案
相关题目
5.下列说法正确的是( )
| A. | CO(NH2)2属于复合肥料 | |
| B. | 农业上把硫酸铵和熟石灰固体混合使用可使肥效提高 | |
| C. | 开发低毒性,低残留的农药代替现有农药 | |
| D. | 为了促进农作物的生长,可以大量施用化肥 |
6.水是生命活动不可缺少的物质,下列有关水污染的防治措施不正确的是( )
| A. | 生活污水经处理后排放 | |
| B. | 禁止含磷洗涤剂的使用 | |
| C. | 合理使用农药和化肥 | |
| D. | 为了节约用水造纸厂废水直接排入河中用于农田灌溉 |
3.为增加食品酸味常使用柠檬酸(C6H8O7).有关柠檬酸的说法不正确的是( )
| A. | 柠檬酸(C6H8O7)不属于氧化物 | |
| B. | 氢元素与氧元素的质量比为8:7 | |
| C. | 碳元素的质量分数为37.5% | |
| D. | 一个柠檬酸分子由6个碳原子、8个氢原子和7个氧原子构成 |
10.在以下四种金属中,有一种金属的盐溶液与其它三种金属都能发生置换反应,这种金属是( )
| A. | Al | B. | Cu | C. | Fe | D. | Ag |
20.除去如表所示物质中的杂质(括号内为杂质),所选用试剂及操作均正确的一组是( )
| 选项 | 待提纯的物质 | 选用的试剂 | 操作方法 |
| A | Na2SO4(NaOH) | 稀硫酸 | 加过量的稀硫酸、蒸发结晶 |
| B | NaCl(Na2CO3) | BaCl2溶液 | 加入适量的BaCl2溶液,过滤,将滤渣洗涤、干燥 |
| C | KCl(K2CO3) | 稀盐酸 | 加过量的稀盐酸,蒸发结晶 |
| D | CaO(CaCO3) | 稀盐酸 | 加入足量的稀盐酸,过滤、洗涤、干燥 |
| A. | A | B. | B | C. | C | D. | D |
7.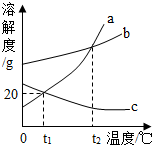 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )| A. | t1℃时,50g水中最多能溶解10ga | |
| B. | 将t1℃时的c的饱和溶液升温,变为不饱和溶液 | |
| C. | a中含有少量b时,可以用降温结晶法提纯a | |
| D. | a、c的饱和溶液从t2℃降温到t1℃时,两种溶液的溶质质量分数:a>c |
4.下列实验操作不正确的是( )
| A. | 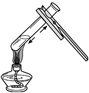 加热液体 | B. | 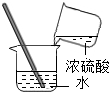 稀释浓硫酸 | C. | 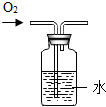 监控O2的流速 | D. |  测 测溶液pH |
5. 氯化铵(NH4Cl)是一种重要的化工原料.
氯化铵(NH4Cl)是一种重要的化工原料.
(1)氯化铵可用作氮肥.
(2)氯化铵的溶解度如下表所示:
20℃时,向盛有37.2g NH4Cl的烧杯中,加入100g的水,充分溶解后形成溶液的是饱和溶液(填“饱和”或“不饱和”).
(3)如图所示,小烧杯中盛放的是(2)中所得的溶液.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.氢氧化钠 C.硝酸铵 D.氧化钙.
 氯化铵(NH4Cl)是一种重要的化工原料.
氯化铵(NH4Cl)是一种重要的化工原料.(1)氯化铵可用作氮肥.
(2)氯化铵的溶解度如下表所示:
| 温度/℃ | 0 | 20 | 40 | 60 | 80 | 100 |
| 溶解度/g | 29.4 | 37.2 | 45.8 | 55.2 | 65.6 | 77.3 |
(3)如图所示,小烧杯中盛放的是(2)中所得的溶液.若将少量的下列物质分别小心地加入到大烧杯的水中,不断搅拌,一定能够使小烧杯中有固体析出的是AC(填字母).
A.冰 B.氢氧化钠 C.硝酸铵 D.氧化钙.