题目内容
7.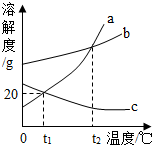 如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )
如图是a、b、c三种物质的溶解度曲线.据此判断,下列说法错误的是( )| A. | t1℃时,50g水中最多能溶解10ga | |
| B. | 将t1℃时的c的饱和溶液升温,变为不饱和溶液 | |
| C. | a中含有少量b时,可以用降温结晶法提纯a | |
| D. | a、c的饱和溶液从t2℃降温到t1℃时,两种溶液的溶质质量分数:a>c |
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:A、t1℃时,a物质的溶解度是20g,所以50g水中最多能溶解10ga,故A正确;
B、c物质的溶解度随温度的升高而减小,所以将t1℃时的c的饱和溶液升温,仍为饱和溶液,故B错误;
C、a物质的溶解度受温度影响较大,所以a中含有少量b时,可以用降温结晶法提纯a,故C正确;
D、降低温度a会析出晶体,b物质不会,a、c的饱和溶液从t2℃降温到t1℃时,a按照t1℃时的溶解度计算,c按照t2℃时的溶解度计算,所以两种溶液的溶质质量分数:a>c,故D正确.
故选:B.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
17.镁及其化合物在生产、生活中应用广泛.
(1)从海水中提取金属镁,可按图1流程进行:

①下列说法正确的是B(选填字母).
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是:电解产生的Cl2用于生产HCl,与Mg(OH)2发生中和反应.
(2)某化学兴趣小组对某种碱式碳酸镁晶体的组成进行探究.
【查阅资料】①碱式碳酸镁晶体可以表示为xMgCO3•yMg(OH)2•zH2O;
②Mg(OH)2、MgCO3受热均能分解生成对应的氧化物;
③碱石灰是固体氢氧化钠和生石灰等物质的混合物.
【设计实验】该小组同学设计了图2所示的实验装置,假设每步反应和吸收均进行完全.
【进行实验】取23.3g碱式碳酸镁晶体进行实验,步骤如下:
①连接好装置并检查气密性.
②装入药品,打开活塞K,通入一段时间空气.
③分别称量装置C、D的质量(数据见上表).
④关闭活塞K,点燃酒精灯,使碱式碳酸镁晶体完全分解.
⑤停止加热,同时打开活塞K,通入空气至恢复到室温.
⑥再次分别称量装置C、D的质量(数据见表).
【实验分析】
①装置A的作用为除去空气中的二氧化碳和水,装置D的作用为吸收反应生成的二氧化碳.
②反应后,装置B中的剩余固体是MgO,质量为10g.
③该碱式碳酸镁晶体[xMgCO3•yMg(OH)2•zH2O]中,x:y:z=4:1:4
(填最简整数比).
(1)从海水中提取金属镁,可按图1流程进行:

①下列说法正确的是B(选填字母).
A.步骤Ⅰ通过一步反应即可实现
B.步骤Ⅱ、Ⅲ、Ⅳ的目的是从海水中提纯氯化镁
C.步骤Ⅴ中化学能转化为电能
D.该流程涉及的基本反应类型有4种
②该流程中采取的一种降低成本且减少污染的措施是:电解产生的Cl2用于生产HCl,与Mg(OH)2发生中和反应.
(2)某化学兴趣小组对某种碱式碳酸镁晶体的组成进行探究.
【查阅资料】①碱式碳酸镁晶体可以表示为xMgCO3•yMg(OH)2•zH2O;
②Mg(OH)2、MgCO3受热均能分解生成对应的氧化物;
③碱石灰是固体氢氧化钠和生石灰等物质的混合物.
【设计实验】该小组同学设计了图2所示的实验装置,假设每步反应和吸收均进行完全.
| 装置C的质量/g | 装置D的质量/g | |
| 步骤③ | 292.4 | 198.2 |
| 步骤⑥ | 296.9 | 207.0 |
①连接好装置并检查气密性.
②装入药品,打开活塞K,通入一段时间空气.
③分别称量装置C、D的质量(数据见上表).
④关闭活塞K,点燃酒精灯,使碱式碳酸镁晶体完全分解.
⑤停止加热,同时打开活塞K,通入空气至恢复到室温.
⑥再次分别称量装置C、D的质量(数据见表).
【实验分析】
①装置A的作用为除去空气中的二氧化碳和水,装置D的作用为吸收反应生成的二氧化碳.
②反应后,装置B中的剩余固体是MgO,质量为10g.
③该碱式碳酸镁晶体[xMgCO3•yMg(OH)2•zH2O]中,x:y:z=4:1:4
(填最简整数比).
18.根据复分解反应发生的条件,判断稀硫酸与下表中的四种化合物的溶液之间能否发生反应,将表中内容补充完整.
[提出问题]稀硫酸与氢氧化钠溶液的反应没有没有观察到明显现象,是否真的发生了反应?
[实验方案]小丽同学设计实验方案进行探究,证明氢氧化钠溶液与稀硫酸发生了反应,请你和她一起完成实验报告.
[实验结论]稀硫酸与氢氧化钠溶液发生了反应;
[反思评价]小丽结合所学知识,认为初中常见的酸碱之间一定能发生复分解反应,她判断的依据是酸与碱生成盐和水,符合复分解反应发生的条件.
[拓展应用]为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应.有关实验数据如表.
请计算:该纯碱样品中碳酸钠的质量分数为多少?
| 氢氧化钠 | 氯化钠溶液 | 碳酸钾溶液 | 硫酸钡溶液 | |
| 稀硫酸 | 能反应 | 不能反应 | 能反应 | 能反应 |
| 判断依据 | 有水生成 | 没有水、气体、沉淀生成 | 有气体和水生成 | 有沉淀生成 |
[实验方案]小丽同学设计实验方案进行探究,证明氢氧化钠溶液与稀硫酸发生了反应,请你和她一起完成实验报告.
| 实验操作 | 实验现象 |
| ①向试管中加入约2mL稀氢氧化钠溶液,滴加2滴酚酞溶液 | 溶液变为红色 |
| ②向①所得溶液中滴加过量稀硫酸 | 红色逐渐变浅至消失 |
[反思评价]小丽结合所学知识,认为初中常见的酸碱之间一定能发生复分解反应,她判断的依据是酸与碱生成盐和水,符合复分解反应发生的条件.
[拓展应用]为了测定某纯碱样品中碳酸钠的质量分数,取该样品与足量稀盐酸在烧杯中反应.有关实验数据如表.
| 反应前 | 反应后 | ||
| 实验数据 | 烧杯和稀盐酸的质量/g | 纯碱样品的质量/g | 烧杯和其中混合物的质量/g |
| 120 | 12 | 127.6 | |
19.某化学兴趣小组做完“木炭还原氧化铜”的实验后,取4.0g混合物放入烧杯中,加入一定质量溶质质量分数为7.3%的稀盐酸,恰好得到蓝色滤液.有关数据如下表:
(1)过滤所得滤渣中一定含有铜.
(2)计算固体混合物中氧化铜的质量.
| 反应前物质的质量/g | 反应后物质的质量/g | |
| 固体混合物 | 稀盐酸 | 蓝色滤液 |
| 4.0 | 未知质量 | 10.8 |
(2)计算固体混合物中氧化铜的质量.
16.下列化学符号所表示的意义错误的是( )
| A. | N2:可以表示一个氮气分子 | B. | Cu2+:可以表示铜单质 | ||
| C. | C:可以表示一个碳原子 | D. | H2O:可以表示水这种物质 |

 小萌来到阳台整理花草.
小萌来到阳台整理花草.