题目内容
3.如图所示的仪器和装置,可用于实验室制取氧气,请回答有关问题: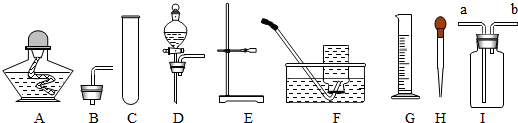
(1)装置A名称酒精灯,用途给物质加热;装置G名称量筒.
(2)用高锰酸钾制取氧气,该反应的化学方程式是2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑,其气体发生装置可选择图中的ABCE(填标号)组合.验证氧气的方法:将带火星的木条伸入瓶内,若木条复燃则是氧气.
(3)装置B、C组合或C、D组合都可以用于实验室制取二氧化碳,比较这两个装置的不同,指出C、D装置组合的一个突出优点可控制反应速率.若用如图I所示的装置收集二氧化碳,气体应从a(“a”或“b”)端通入.
(3)在量取水的操作中,当水面接近所需刻度时,应改用胶头滴管(填上述仪器的名称)加水至所需刻度.
(4)用F装置来收集的气体具有什么性质不易溶于水或不溶于水,且不与水反应.除了氧气,还有什么气体可用F装置来收集氢气(合理均可).
分析 (1)据仪器的名称和用途解答;
(2)据反应原理书写方程式,该反应属于固体加热型,据此选择仪器,验证氧气用带火星的木条伸入瓶内,观察木条是否复燃进行判断;
(3)C中的分液漏斗可逐滴滴加液体,可用来控制反应速率,二氧化碳密度比空气大,所以应从长管进气,将空气挤压到集气瓶上部排出;
(4)量取一定体积的水,当水面接近所需刻度时,应改用胶头滴管加水至所需刻度;
(5)排水法收集不易溶于水或不溶于水的气体,且气体不与水反应;氢气难溶于水,也不与水反应,可用此法收集.
解答 解:(1)A是用于给物质加热的酒精灯,G是量筒;
(2)加热高锰酸钾生成锰酸钾、二氧化锰和氧气,反应方程式是:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;该反应属于固体加热型,所以应选择加热的酒精灯,装药品的试管,固定试管的铁架台,及导出气体的带塞子的导管;验证氧气用带火星的木条伸入瓶内,观察木条是否复燃进行判断;
(3)CD装置组合与BC装置组合的不同之处在于C中有添加液体的分液漏斗,液漏斗可逐滴滴加液体,从而可控制反应物的量,进而控制反应速率,这是C、D装置组合的一个突出优点,二氧化碳密度比空气大,所以应从长管进气,将空气挤压到集气瓶上部排出;
(4)量取一定体积的水,当水面接近所需刻度时,应改用胶头滴管加水至所需刻度;
(5)排水法收集不易溶于水或不溶于水的气体,且气体不与水反应;氢气、甲烷难溶于水,也不与水反应,可用此法收集;
故答案为:(1)酒精灯;给物质加热;量筒;
(2)2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑;ABCE;将带火星的木条伸入瓶内,若木条复燃则是氧气;
(3)可控制反应速率;a;
(4)胶头滴管;
(5)不易溶于水或不溶于水,且不与水反应;氢气(合理均可).
点评 本题考查知识比较基础,掌握实验室制取氧气的反应原理、检验氧气的方法,收集气体的方法等知识,即可顺利解答.

| 稀盐酸的用量 | 第一次加入10g | 第二次加入10g | 第三次加入10g | 第四次加入10g |
| 剩余固体的质量 | 3.0g | 2.0g | 1.0g | 0.4g |
(1)4g的石灰石样品中含有杂质多少克?
(2)该石灰石样品中的碳酸钙质量分数是多少?
(3)4g石灰石样品与足量的稀盐酸反应,生成二氧化碳多少克?
