题目内容
8.氢氧化钙20度时溶解度大于0.15克,将0.1克CaO完全溶于99.9克水,所得溶液中溶质的质量分数>0.1%.(填“<”、“>”或“=”)分析 氧化钙与水反应生成的氢氧化钙是微溶于水的物质,且溶质质量增加,据此进行解答.
解答 解:CaO完全溶于克水中,生成氢氧化钙,氢氧化钙的质量比CaO大.且氢氧化钙20度时溶解度大于0.15克,所以将0.1克生成微溶于水的氢氧化钙,溶质质量增加,所得溶液中溶质的质量分数>0.1%.
故填:>.
点评 本题考查了溶质的质量分数.解题时要注意:氢氧化钙是微溶于水的物质.

练习册系列答案
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案 浙大优学小学年级衔接导与练浙江大学出版社系列答案
浙大优学小学年级衔接导与练浙江大学出版社系列答案
相关题目
18.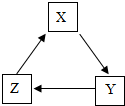 下列各组物质通过一步反应就能实现如图转化的是( )
下列各组物质通过一步反应就能实现如图转化的是( )
 下列各组物质通过一步反应就能实现如图转化的是( )
下列各组物质通过一步反应就能实现如图转化的是( )| X | Y | Z | |
| A | H2O | O2 | CO2 |
| B | Ca(OH)2 | NaOH | NaCl |
| C | AgNO3 | Ba(NO3)2 | BaSO4 |
| D | Fe | FeCl2 | Fe2O3 |
| A. | A | B. | B | C. | C | D. | D |
19.把炭和氧化铜组成的混合物隔绝空气加热,充分反应后称量所得剩余固体的质量为112g,向此剩余固体中加入200g稀硫酸,稀硫酸恰好被完全反应,过滤后所得滤渣呈红色.同时将反应所得的气体全部通入含溶质37g的澄清石灰水中,得到沉淀25g.下列有关说法不正确的是( )
| A. | 生成气体的质量可能是11克或33克 | |
| B. | 滤渣中的红色物质可能是32克或96克 | |
| C. | 参与反应的氧化铜质量可能是40克或120克 | |
| D. | 稀硫酸的溶质质量可能是38.4克或115.2克 |
13.下表是硝酸钾在某些温度的溶解度,将60℃时100g24%的硝酸钾溶液变成饱和溶液可以采用的方法是:加入硝酸钾59.6g;或降低温度到20℃恰好饱和.
| 温度(℃) | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| 溶解度(g/100g水) | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 | 169 | 202 | 246 |
17.关于有机合成材料下列说法错误的是.
| A. | 有机合成材料都是高分子材料 | |
| B. | 焚烧聚乙烯塑料会造成环境污染 | |
| C. | 使用过的塑料、橡胶应回收利用 | |
| D. | 棉花、羊毛、聚乙烯、橡胶都是合成材料 |
8.金属材料在生产、生活中的应用非常广泛.
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的B(填序号).
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的水和氧气发生化学反应的过程.
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)金属是一种重要的材料,人类的生活和生产都离不开金属.下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.
根据图1中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列③⑤有关.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性;④金属的延展性;⑤金属冶炼的难易程度.
(5)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是铁片、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和硫酸亚铁.
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(6)炼铁的原理是利用一氧化碳与氧化铁反应,其反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在实验室里,可用图2所示装置进行实验:实验中玻璃管内的粉末由红色色变黑色,红色粉末氧化铁中的铁元素的化合价为+3价.
(7)某钢铁厂每天需消耗5 000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁2587.1t.(计算结果保留1位小数)
(8)某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶与水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
请你认真分析数据,回答下列问题:
①乙同学所用的稀硫酸与铁的样品恰好完全反应?
②计算铁的样品中铁的质量分数.(写出详细的计算过程)
(1)吃火锅用的锅体是由铜合金制造的,主要是因为铜合金具有很好的B(填序号).
A.导电性 B.导热性 C.延展性
(2)金属锈蚀造成浪费.铁制品锈蚀的过程,实际上是铁与空气中的水和氧气发生化学反应的过程.
(3)目前世界上已有50%以上的废钢铁得到回收利用,其目的是A.
A.节约金属资源 B.合理开采矿物 C.防止钢铁生锈
(4)金属是一种重要的材料,人类的生活和生产都离不开金属.下表表示了金属活动性顺序表中铜、锡、铁和铝元素被人类大规模开发、利用的大致年限.

根据图1中数据和有关的化学知识,你认为金属大规模开发、利用的先后顺序跟下列③⑤有关.
①地壳中金属元素的含量;②金属的导电性;③金属的活动性;④金属的延展性;⑤金属冶炼的难易程度.
(5)实验室有锌片、铁片、铜片、稀硫酸、硫酸锌溶液、硫酸亚铁溶液和硫酸铜溶液7种物质,小红选择合适的物质,设计了以下三种方法对锌、铜、铁的金属活动性顺序进行验证.
①方法一所选用的3种物质是铁片、硫酸锌溶液和硫酸铜溶液.
②方法二所选用的3种物质是锌片、铜片和硫酸亚铁.
③方法三所选用4种物质是锌片、铁片、铜片和稀硫酸.
(6)炼铁的原理是利用一氧化碳与氧化铁反应,其反应的化学方程式为Fe2O3+3CO$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,在实验室里,可用图2所示装置进行实验:实验中玻璃管内的粉末由红色色变黑色,红色粉末氧化铁中的铁元素的化合价为+3价.
(7)某钢铁厂每天需消耗5 000t含Fe2O380%的赤铁矿石,该厂理论上可日产含Fe 98%的生铁2587.1t.(计算结果保留1位小数)
(8)某兴趣小组的同学对一批铁的样品(含有杂质,杂质不溶与水,也不与稀硫酸反应)进行分析,甲、乙、丙三位同学分别进行实验,其中一位同学所用的稀硫酸与铁样品恰好完全反应,实验数据如表:
| 甲 | 乙 | 丙 | |
| 烧杯+稀硫酸的质量 | 200 | 150 | 150 |
| 加入铁的样品的质量 | 9 | 9 | 14 |
| 充分反应后,烧杯+剩余物的质量 | 208.7 | 158.7 | 163.7 |
①乙同学所用的稀硫酸与铁的样品恰好完全反应?
②计算铁的样品中铁的质量分数.(写出详细的计算过程)