题目内容
13.氨基酸是形成蛋白质的基本单元,某氨基酸的相对分子质量为89,其中氮元素的质量分数为15.73%,则一个该氨基酸分子中含有的氮原子个数为( )| A. | 1 | B. | 2 | C. | 3 | D. | 4 |
分析 根据题意,某氨基酸的相对分子质量为89,其中氮元素的质量分数为15.73%,据此结合化合物中某元素的质量=该化合物的质量×该元素的质量分数,进行分析解答.
解答 解:某氨基酸的相对分子质量为89,其中氮元素的质量分数为15.73%,则一个该氨基酸分子中含有的氮原子个数为89×15.73%÷14≈1.
故选:A.
点评 本题难度不大,掌握化合物中某元素的质量=该化合物的质量×该元素的质量分数是正确解答本题的关键.

练习册系列答案
相关题目
3.下列净化水的方法中发生了化学反应的是( )
| A. | 用活性炭来净化水 | B. | 通过过滤来净化水 | ||
| C. | 用明矾来净化水 | D. | 通过蒸馏来净化水 |
1.下列各组物质中,相互不能发生反应的是( )
| A. | 氢氧化钠溶液和硫酸 | B. | 氧化铁和盐酸 | ||
| C. | 三氧化硫和氢氧化钠溶液 | D. | 盐酸和二氧化硫 |
8.生活中铁制品容易锈蚀,某课外学习小组探究铁生锈的条件.用洁净无锈的铁钉、试管、经煮沸迅速冷却的蒸馏水、植物油、棉花和干燥剂氯化钙,实验装置图如图.
一周后观察到只有A中的铁钉生锈,而B、C中铁钉均无变化,请回答下列问题:
(1)在B试管中蒸馏水需要煮沸并覆盖一层植物油的目的是排除水中溶解的氧气,防止铁钉与氧气(或空气)接触.
(2)实验A和实验B对比,证明了铁钉生锈需要接触氧气.
(3)某同学将A试管中生锈的铁钉浸入装有足量的稀盐酸的试管中,发现铁锈逐渐溶解,溶液由无色逐渐变成黄色(FeCl3),没有气泡产生.这是因为Fe2O3+6HCl═2FeCl3+3H2O(用化学方程式表示);一段时间后,该同学发现试管中有气泡产生,此时发生反应的化学方程式是Fe+2HCl═FeCl2+H2↑.
| 实验操作 | 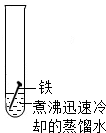 A | 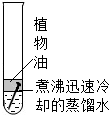 B | 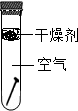 C |
(1)在B试管中蒸馏水需要煮沸并覆盖一层植物油的目的是排除水中溶解的氧气,防止铁钉与氧气(或空气)接触.
(2)实验A和实验B对比,证明了铁钉生锈需要接触氧气.
(3)某同学将A试管中生锈的铁钉浸入装有足量的稀盐酸的试管中,发现铁锈逐渐溶解,溶液由无色逐渐变成黄色(FeCl3),没有气泡产生.这是因为Fe2O3+6HCl═2FeCl3+3H2O(用化学方程式表示);一段时间后,该同学发现试管中有气泡产生,此时发生反应的化学方程式是Fe+2HCl═FeCl2+H2↑.
18.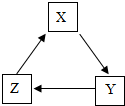 下列各组物质通过一步反应就能实现如图转化的是( )
下列各组物质通过一步反应就能实现如图转化的是( )
 下列各组物质通过一步反应就能实现如图转化的是( )
下列各组物质通过一步反应就能实现如图转化的是( )| X | Y | Z | |
| A | H2O | O2 | CO2 |
| B | Ca(OH)2 | NaOH | NaCl |
| C | AgNO3 | Ba(NO3)2 | BaSO4 |
| D | Fe | FeCl2 | Fe2O3 |
| A. | A | B. | B | C. | C | D. | D |
5.实验现象与结论对应正确的是( )
| A. | 某固体中加入稀硫酸,产生气泡,该固体为活泼金属 | |
| B. | 某溶液中滴加酚酞试剂,不变色,该溶液为酸性溶液 | |
| C. | 某溶液进行焰色反应,火焰呈黄色,该溶液中含有钠元素 | |
| D. | 某溶液中滴加氯化钡和稀硝酸,产生白色沉淀,该溶液中含有硫酸盐 |