题目内容
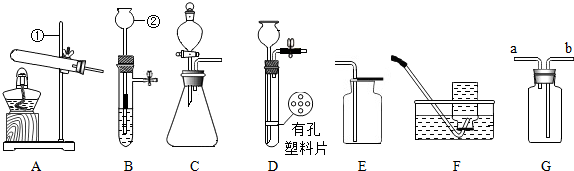
16.化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动.【提供资料】①二氧化碳与过氧化钠反应生成氧气和另一种物质.
②碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)与盐酸反应均能生成CO2.
③2Na2O2+2H2O═4NaOH+O2↑.
(1)证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气.
同学们在老师的指导下设计了如下图所示的装置.
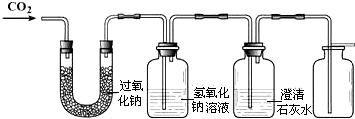
①证明氧气已经收集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满.
②氢氧化钠溶液的作用是除去未反应的二氧化碳,澄清石灰水的作用是检验二氧化碳是否除尽.
(2)探究二氧化碳与过氧化钠反应生成的另一种物质.
【猜想与假设】下面是同学们提出的3种猜想.
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
通过对反应物中有关元素的组成分析,你认为猜想1、2是不正确的,
理由是两种反应物中均无氢元素.
【进行实验】同学们通过以下实验验证了另一种物质,请完成下述实验报告.
| 实验操作 | 实验现象 | 实验结论 |
| 取少量CO2与Na2O2反应后的固体于 试管中,加入适量的稀盐酸, 并将生成的气体导入澄清石灰水中 | 有大量气泡产生,澄清石灰水变浑浊. | 猜想3是 正确的. |
分析 (1)①根据氧气的验满方法分析解答;
②根据二氧化碳能使澄清的石灰水变浑浊分析解答;
(2)【作出猜想】根据质量守恒定律可以知道反应前后元素的种类不变,对作出的猜想做出合理的判断与解释;
【进行实验】根据题给条件及所学知识完成该实验的现象和结论;
【反思与交流】根据质量守恒定律和题中的水也能和过氧化钠反应生成氧气,可以作出解答.
解答 解:(1)①检验氧气是否集满的方法是将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满;
②二氧化碳能澄清石灰水变浑浊,澄清石灰水的作用是检验二氧化碳是否除尽;
(2)【作出猜想】根据质量守恒定可以知道:二氧化碳与过氧化钠都不含氢元素,所以不可能生成含有氢元素的碳酸或氢氧化钠,猜想1、2是不正确的;
【进行实验】检验碳酸钠常用稀盐酸或是稀硫酸与之反应,如果生成气体,则把生成的气体通入石灰水观察现象,然后作出判断,所以
| 实验步骤 | 实验现象 | 实验结论 |
| 将CO2与Na2O2反应后的固体取少量于试管中,加入 稀盐酸(或稀硫酸等, 把产生的气体通入足量的澄清石灰水中 | ①有大量气泡产生 ②澄清石灰水变浑浊 | 猜想3是正确的 |
故故答案为:(1)①将带火星的木条放在集气瓶口,若木条复燃,则氧气已收集满;
②检验二氧化碳是否除尽;
(2)【作出猜想】1、2,两种反应物中均无氢元素;
【进行实验】稀盐酸,3;
【反思与交流】不同意,因为人呼出的气体中含有氧气和水蒸气等,水也能与过氧化钠反应生成氧气.
点评 熟练掌握实验室中制取二氧化碳的装置,并记住化学方程式:CaCO3+2HCl=CaCl2+H2O+CO2↑,能够熟练的应用盐酸和石灰水对碳酸盐做出检验.

练习册系列答案
 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案
相关题目
14.下列现象能说明铁在氧气中燃烧是一个化学变化的本质现象是( )
| A. | 燃烧 | B. | 火星四射 | C. | 放热 | D. | 生成黑色固体 |
7.如图所示的化学实验基本操作中,正确的是( )
| A. |  点燃酒精灯 | B. |  倾倒液体 | C. | 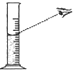 量取液体 | D. |  闻气体气味 |
11.下列说法正确的是( )
| A. | 铜是目前世界年产量最高的金属 | |
| B. | 日常使用的金属材料大多数是合金 | |
| C. | 铝是地壳中含量最多的金属元素 | |
| D. | 大多数金属元素在自然界中以单质形式存在 |
1.下列装置或实验设计使用不恰当的是( )
| A. | 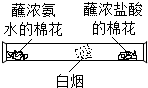 探究分子运动 | B. | 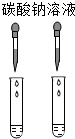 鉴别盐酸和稀硫酸 | ||
| C. | 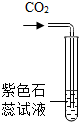 探究二氧化碳的性质 | D. | 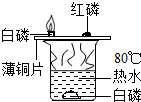 探究燃烧的三个条件 |
8.研究金属的腐蚀对资源的利用和保护意义重大.
(1)为了探究铁锈蚀的条件,进行如图1所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.
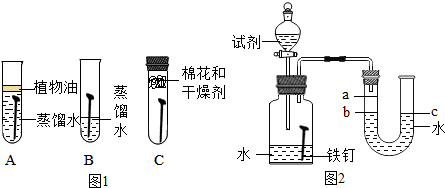
①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是把溶解在水中的氧气排出.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②氧气的含量;③水溶液的导电性.
【实验】每次取两套如图2所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
(3)若将两根铁钉分别放入两支试管中,在一支试管中加入稀硫酸,另一支试管中加入稀盐酸,观察到两支试管内均有大量气泡产生,铁钉逐渐溶解,在酸溶液中被快速腐蚀.
【反思与提高】
根据该探究实验以及你所学的知识,判断下列说法正确的是AC(填序号).
A.金属的腐蚀是指金属单质与其它物质发生化学反应的过程
B.金属越活泼,就越容易被锈蚀
C.金属腐蚀不一定要有氧气参加.
(1)为了探究铁锈蚀的条件,进行如图1所示实验.经过一周后观察,试管A和C中的铁钉无明显变化,试管B中的铁钉明显锈蚀.

①通过实验发现:铁锈蚀是铁与氧气和水发生化学反应的过程.
②A中加入的蒸馏水要事先煮沸,其目的是把溶解在水中的氧气排出.
(2)家中的刀具若沾有食盐水锈蚀更快.为了进一步探究影响铁锈蚀速率的因素,做了如下的实验.
【提出问题】铁锈蚀速率与哪些因素有关.
【查阅资料】①物质溶解在水中得到的混合物称为水溶液,如氯化钠溶解在水中得到氯化钠溶液,乙醇溶解在水中得到乙醇溶液.
②氯化钠溶液能导电;乙醇溶液不能导电.
【猜想】铁的锈蚀速率与下列因素有关:
①反应时的温度;②氧气的含量;③水溶液的导电性.
【实验】每次取两套如图2所示的装置,编号为I、II.向两套装置中分别装入质量、大小相同的铁钉和等体积的蒸馏水,进行如下三组对比实验(实验开始时,各瓶内气体压强保持一致).
| 影响因素 | 实验设计 | 实验现象 | 实验结论及解释 |
| ①温度 | 装置I放入25℃恒温环境中,装置II放入40℃恒温环境中. | 两套装置中铁钉均锈蚀,且U型管中液面均由b处上升至a处,则所需时间I>II. | 锈蚀的速率I<II;铁的锈蚀速率与反应时的温度有关,温度越高,铁的锈蚀速率越快. |
| ②氧气含量 | 在相同温度下,向I、II两套装置的集气瓶中分别通入氧气和空气. | 铁钉均锈蚀,且U型管中液面由b处上升至a处所需时间I<II. | 铁的锈蚀速率与氧气的含量有关,氧气的含量越多,铁的锈蚀越快. |
| ③水溶液的导电性 | 在相同温度下,装置I集气瓶中加入10mL氯化钠溶液;装置II集气瓶中加入10mL乙醇. | 两套装置中铁钉均锈蚀; 且U型管中液面均由b处上升至a处,则所需时间I<II. | 铁的锈蚀速率与水溶液的导电性有关,在能导电的溶液中,锈蚀的速率加快. |
【反思与提高】
根据该探究实验以及你所学的知识,判断下列说法正确的是AC(填序号).
A.金属的腐蚀是指金属单质与其它物质发生化学反应的过程
B.金属越活泼,就越容易被锈蚀
C.金属腐蚀不一定要有氧气参加.
6.下列说法正确的是( )
| A. | 化学变化过程中一定同时发生物理变化 | |
| B. | 物理变化过程中一定同时发生化学变化 | |
| C. | 化学变化和物理变化一定同时发生 | |
| D. | 化学变化中一定伴随放热、发光、放出气体、生成沉淀等现象 |