题目内容
12. 硝酸钾、氯化钾固体的溶解度曲线如图:
硝酸钾、氯化钾固体的溶解度曲线如图:(1)t1℃时KNO3饱和溶液的质量分数=KCl饱和格液的质量分数(填“>”、“<”或“=”).
(2)t2℃时,在盛有50k水的烧杯中,加入30gKCl固体(填“KN03”或“KCl”),充分搅拌后形成饱和溶液.
(3)从曲线可以看出,KN03固体的溶解度受温度影响更大.
(4)想从KNO3的饱和溶液中获得KNO3固体,可采用蒸发或降低温度的方法.
分析 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.
解答 解:(1)通过分析溶解度曲线可知,t1℃时,硝酸钾的溶解度等于氯化钾的溶解度,所以KNO3饱和溶液的质量分数=KCl饱和溶液的质量分数;
(2)t2℃时,氯化钾的溶解度是60g,所以在盛有50k水的烧杯中,加入30gKCl固体,充分搅拌后形成饱和溶液;
(3)通过分析溶解度曲线可知,KN03固体的溶解度受温度影响更大;
(4)硝酸钾的溶解度随温度的升高而增大,所以从KNO3的饱和溶液中获得KNO3固体,可采用蒸发或降低温度的方法.
故答案为:(1)=;
(2)KCl;
(3)KNO3;
(4)蒸发,降低温度.
点评 本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度曲线来解决相关的问题,从而培养分析问题、解决问题的能力.

练习册系列答案
 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案 名题训练系列答案
名题训练系列答案
相关题目
2.下列除去杂质(括号内为杂质)的方法正确的是( )
| A. | CO(CO2):通过灼热的CuO | |
| B. | 铁粉(氧化铜):加入足量的稀硫酸 | |
| C. | NaCl溶液(硫酸钠):加入适量的BaCl2溶液 | |
| D. | NaOH溶液(Na2CO3):加入适量的稀盐酸 |
3.实验室中有一瓶久置的熟石灰,同学们猜想瓶子熟石灰可能已变质,他们通过以下实验测定了其中氢氧化钙的质量分数.取10g熟石灰样品于一只洁净的烧杯中,向其中逐滴滴加15%的稀盐酸至不再产生气泡,测得加入的盐酸与烧杯中物质的质量关系如表.
(1)实验中若要用36.5%的浓盐酸(密度:1.2g/ml),配置15%的稀盐酸30g,需要36.5%的浓盐酸的体积为10.3mL.(精确到0.1)
(2)生成二氧化碳的质量为1.1g.
(3)计算样品中氢氧化钙的质量分数.
| 加入稀盐酸的质量 | 0 | 10 | 20 | 30 |
| 烧杯中物质的质量 | 10 | 19.8 | 28.9 | 38.9 |
(2)生成二氧化碳的质量为1.1g.
(3)计算样品中氢氧化钙的质量分数.
20.下列实验室常用仪器制作材料为有机合成材料的是( )
| A. |  集气瓶 | B. |  坩埚钳 | C. |  塑料药匙 | D. |  石棉网 |
17.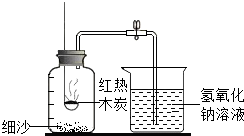 某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
(1)写出氢氧化钠溶液吸收二氧化碳发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是红磷只能与氧气反应且生成物为固体.
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理.
【查阅资料】木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%.
乙同学又利用上述装置设计了如下实验,请你填写如表.
【交流与反思】
(3)请分析步骤2中,你选择的可燃物的理由三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花.
(4)由此实验你对物质燃烧的条件有何新的认识可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气).
(5)从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
 某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.
某研究性学习小组在“利用燃碳法测定空气中氧气的体积分数”的实验时(如图装置),发现一个现象:氢氧化钠溶液吸收生成的二氧化碳后,进入集气瓶中氢氧化钠溶液的体积分数仍然小于$\frac{1}{5}$.(1)写出氢氧化钠溶液吸收二氧化碳发生反应的化学方程式CO2+2NaOH=Na2CO3+H2O.
(2)教材中利用燃烧红磷法测定空气中氧气体积分数,选择该药品的原因是红磷只能与氧气反应且生成物为固体.
【提出问题】是什么原因导致测量不准确呢?
【猜想与假设】他们分别作了如下猜想:
甲同学:可能是木炭取的量过少;
乙同学:可能是木炭燃烧没有消耗完集气瓶中的氧气;
小组同学发现实验结束后,燃烧匙中还有残留的黑色固体,都认为甲同学的猜想不合理.
【查阅资料】木炭、棉花和蜡烛在密闭容器内燃烧停止后,残留氧气的体积分数高达14.0%、8.0%和16.0%.
乙同学又利用上述装置设计了如下实验,请你填写如表.
| 实验步骤 | 实验现象 | 实验结论 |
| 1将足量木炭点燃,迅速插入集气瓶中 | 棉花继续燃烧 | 木炭燃烧没有消耗完集气瓶中的氧气. |
| 2待冷却后,将燃着的棉花(填“棉花”或“蜡烛”)再伸入该集气瓶中 |
(3)请分析步骤2中,你选择的可燃物的理由三种物质燃烧时需要的氧气浓度大小依次为蜡烛>木炭>棉花.
(4)由此实验你对物质燃烧的条件有何新的认识可燃物燃烧需要的氧气要达到一定的浓度(或可燃物燃烧需要足够的氧气).
(5)从木炭燃烧反应的产物分析你认为测量结果小于$\frac{1}{5}$的理由还有可能是木炭燃烧生成了CO.
2.下列关于Mg、Mg2+两种粒子的判断中不正确的是( )
| A. | 核电荷数相同 | B. | 质量几乎相等 | C. | Mg2+比Mg稳定 | D. | 电子层数相同 |