题目内容
19.可溶于水的钡盐[如硝酸钡,氯化钡等]对人体有毒,但是难溶于水也难溶于酸的BaSO4没有毒,还由于它具有不易被X射线透过的特点,在医疗上被用做X射线透视胃肠的内服药剂--“钡餐”.(1)有人认为也可以用BaCO3代替BaSO4来做钡餐,现请你判断,说明理由并写出有关的化学方程式BaCO3+2HCl=BaCl2+H2O+CO2↑
(2)若误食了BaCl2,可用于解毒的药剂是B并写出反应的化学方程式Na2SO4+BaCl2═BaSO4↓+2NaCl.
A.糖水 B.硫酸钠溶液 C.食盐水 D.硫酸镁溶液.
分析 依据可溶性钡盐的毒性、在胃液中的碳酸钡和硫酸钡的溶解性,可以得出本题的正确答案.
解答 解:(1)由于可溶性的氯化钡有毒,碳酸钡与胃液中的盐酸反应生成可溶性的氯化钡,会引起人体中毒,因此不能用碳酸钡代替硫酸钡来做钡餐.
上述反应中碳酸钡与盐酸反应生成氯化钡、水和二氧化碳.
该反应的化学方程式为:BaCO3+2HCl=BaCl2+H2O+CO2↑.
(2)糖水和氯化钠与氯化钡不反应,不能将其转化成不溶性的钡盐,因此糖水和氯化钠不能用作解毒的药剂.
由于不溶性的硫酸钡无毒,氯化钡与硫酸钠反应能生成不溶性的硫酸钡沉淀,因此可以用硫酸钠溶液作解毒的药剂.
由于氯化铜是可溶性的重金属盐,会引起人体中毒,氯化钡与硫酸铜反应尽管能形成不溶性的硫酸钡沉淀,解除氯化钡的毒性,但同时又生成了会使人体中毒的氯化铜,因此硫酸铜不能用作解毒的药剂.
故选B.
答案为:
(1)不能.因为胃酸中含有盐酸,BaCO3与盐酸反应生成可溶性的BaCl2,引起人体中毒.BaCO3+2HCl=BaCl2+H2O+CO2↑;
(2)B.Na2SO4+BaCl2═BaSO4↓+2NaCl.
点评 本题主要考查钡盐和铜盐的溶解性和毒性,难度较大.解答本题时,首先要明确不能用可溶性钡盐代替硫酸钡的原因,其次要明确不能用糖水和食盐水解毒的原因和不能用硫酸铜解毒的原因.

练习册系列答案
相关题目
9.下列能量转化过程中,属于化学变化的是( )
| A. | 风力发电 | B. | 灯泡发光发热 | C. | 火力发电 | D. | 电暖器取暖 |
10.下列有关量的描述正确的是( )
| A. | 空气中氧气的质量分数约为21% | |
| B. | 电解水中两极得到的气体体积比V正:V负为2:1 | |
| C. | 用10mL筒量量取9.25mL蒸馏水 | |
| D. | 一个氢原子的质量为1.67×10-27kg |
4.下列物质属于纯净物( )
| A. | 液氧 | B. | 新鲜的空气 | C. | 干净的豆浆 | D. | 河水 |
11.对下列现象或做法的解释不正确的是( )
| A. | 洒到地面上的酒会使房间充满酒味,说明分子在不断运动 | |
| B. | 膨化食品变得不再松脆,是因为食品可能吸收了空气中的水分 | |
| C. | 用洗洁精洗去餐具上的油污,是因为洗洁精具有乳化作用 | |
| D. | 消防队员用高压水枪喷水灭火,是因为水能降低可燃物的着火点 |
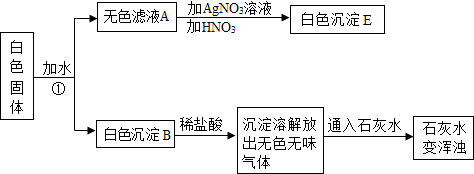
 (1)硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图所示的装置进行实验.已知△
(1)硫酸铵是常用的一种氮肥,现有一种硫酸铵化肥,为测定其中硫酸铵的质量分数,采用如图所示的装置进行实验.已知△