题目内容
6.某兴趣小组同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验:| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 | 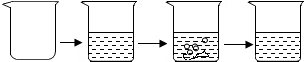 | |||
| 实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中剩余混合物的质量为107.6g |
(1)该实验中生成的二氧化碳的质量是4.4g.
(2)该石灰石样品的纯度是否符合要求?(该石灰石样品中杂质不与盐酸反应也不溶于水)
分析 (1)石灰石中主要成分碳酸钙可以与盐酸反应生成氯化钙、水和气体二氧化碳;随着反应的发生,二氧化碳不断放出而使烧杯内物质质量减小;完全反应前后烧杯中物质质量差为放出气体二氧化碳的质量;
(2)根据反应的化学方程式,可由反应放出二氧化碳的质量计算参加反应的碳酸钙的质量,进而求质量分数.
解答 解:(1)根据质量守恒定律得:反应放出CO2的质量=(100.0g+12.0g)-107.6g=4.4g;
(2)设12.0g石灰石样品中含CaCO3质量为x
CaCO3+2HCl═CaCl2+CO2↑+H2O
100 44
x 4.4g
$\frac{100}{44}=\frac{x}{4.4g}$
x=10.0g
该石灰石样品的纯度为:$\frac{10g}{12g}$×100%=83.3%
因83.3%<85%,所以该石灰石样品的纯度不符合要求.
答:(1)该实验中生成的二氧化碳的质量是4.4g;
(2)该石灰石样品的纯度不符合要求.
点评 根据质量守恒定律,放出气体的反应,反应前各物质的总质量与反应后剩余物质的质量差即为反应放出气体的质量.

练习册系列答案
相关题目
11.下列过程一定包含化学变化的是( )
| A. | 海水晒盐 | B. | 火力发电 | C. | 电灯发光 | D. | 轮胎爆炸 |
18.下列过程发生的变化中,属于物理变化的是( )
| A. |  生石灰溶于水 | B. |  利用风力发电 | C. |  食物的消化 | D. |  塑料的合成 |
15.下列实验操作中,正确的是( )
| A. | 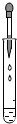 滴加液体 | B. | 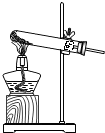 加热液体 | ||
| C. | 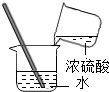 稀释浓硫酸 | D. | 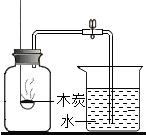 测定空气中氧气的含量 |
16.如表为各物质中所含有的少量杂质及除去这些杂质应选用的试剂或操作方法.正确的一组为( )
| 序号 | 物质 | 杂质 | 除杂质应选用的试剂或操作方法 |
| ① | KNO3溶液 | KOH | 加入FeCl3溶液,并过滤 |
| ② | FeSO4溶液 | CuSO4 | 加入过量铁粉,并过滤 |
| ③ | H2 | CO2 | 通过盛有NaOH溶液的洗气瓶,再通过盛有浓硫酸的洗气瓶 |
| ④ | NaCl | CaCO3 | 溶解、过滤、蒸发 |
| A. | ①②③④ | B. | ③④ | C. | ②③④ | D. | ①②③ |
 A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)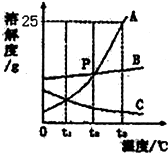 如图是A、B、C三种物质的溶解度曲线.
如图是A、B、C三种物质的溶解度曲线.
