题目内容
11.下列过程一定包含化学变化的是( )| A. | 海水晒盐 | B. | 火力发电 | C. | 电灯发光 | D. | 轮胎爆炸 |
分析 化学变化是指有新物质生成的变化,物理变化是指没有新物质生成的变化,化学变化和物理变化的本质区别是否有新物质生成;据此分析判断.
解答 解:A、海水晒盐过程中没有新物质生成,属于物理变化.
B、火力发电过程中有新物质生成,属于化学变化.
C、电灯发光过程中没有新物质生成,属于物理变化.
D、轮胎爆炸过程中没有新物质生成,属于物理变化.
故选B.
点评 本题难度不大,解答时要分析变化过程中是否有新物质生成,若没有新物质生成属于物理变化,若有新物质生成属于化学变化.

练习册系列答案
 寒假天地重庆出版社系列答案
寒假天地重庆出版社系列答案
相关题目
1.下列有关金属的描述不正确的是( )
| A. | 地壳中含量最多的金属元素是铝 | |
| B. | 车船表面涂油漆可防止生锈 | |
| C. | 废铜屑可全部溶解于过量稀盐酸 | |
| D. | 用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器 |
19.类推是学习过程中常用的思维方法,以下类推结果中正确的是( )
| A. | 因为碱溶液通常呈碱性,所以碱性溶液一定是碱的溶液 | |
| B. | 因为金属铝与稀盐酸反应生成AlCl3和H2,所以金属铁与稀盐酸反应生成FeCl3和H2 | |
| C. | 因为甲烷含碳元素和氢元素,其燃烧产物为二氧化碳和水,乙醇燃烧产物也为二氧化碳和水,所以乙醇中一定也含碳元素和氢元素 | |
| D. | 因为中和反应生成盐和水,所以生成盐和水的反应一定是中和反应 |
6.某兴趣小组同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验:
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是4.4g.
(2)该石灰石样品的纯度是否符合要求?(该石灰石样品中杂质不与盐酸反应也不溶于水)
| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 | 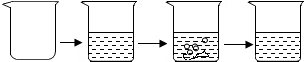 | |||
| 实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中剩余混合物的质量为107.6g |
(1)该实验中生成的二氧化碳的质量是4.4g.
(2)该石灰石样品的纯度是否符合要求?(该石灰石样品中杂质不与盐酸反应也不溶于水)
3.下列实验操作正确的是( )
| A. | 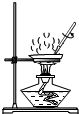 | B. | 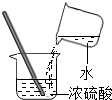 | C. |  | D. | 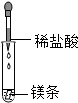 |
20.下列有关物构成的说法不正确的是( )
| A. | Hg由原子构成,H2由分子构成 | |
| B. | 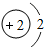 和 和 最外层都有2个电子,化学性质相似 最外层都有2个电子,化学性质相似 | |
| C. | X原子的核内质子数为n,该原子核外电子数也为n | |
| D. | 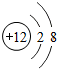 、 、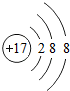 ,分别表示Mg2+和Cl- ,分别表示Mg2+和Cl- |
1.水是生命之源,“爱惜水、保护水”是每个公民的义务和责任.
(1)去年4月25日尼泊尔境内发生地震,高铁酸钾(K2FeO4)可用于灾区饮用水的净化,制备K2FeO4的化学反应方程式为:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,X的化学式为KCl,在K2FeO4的化学式中标出中Fe元素的化合价+6.
(2)污水处理是防止水污染的重要措施之一,某工厂甲、乙两车家产生的污水中各含有以下四种物质中的两种:Ba(NO3)2,KOH,K2SO4,HNO3,用石蕊试液和氯化钡溶液分别对两车间污水进行检测,现象如表:
则甲车间产生的污水含有上述四种物质中的KOH、K2SO4,若反应池内各物质均恰好完全反应,排放液中的溶质是硝酸钾.
(1)去年4月25日尼泊尔境内发生地震,高铁酸钾(K2FeO4)可用于灾区饮用水的净化,制备K2FeO4的化学反应方程式为:2Fe(OH)3+3Cl2+10KOH=2K2FeO4+6X+8H2O,X的化学式为KCl,在K2FeO4的化学式中标出中Fe元素的化合价+6.
(2)污水处理是防止水污染的重要措施之一,某工厂甲、乙两车家产生的污水中各含有以下四种物质中的两种:Ba(NO3)2,KOH,K2SO4,HNO3,用石蕊试液和氯化钡溶液分别对两车间污水进行检测,现象如表:
| 石蕊试液 | 氯化钡溶液 | |
| 甲车间 | 变蓝色 | 产生白色沉淀 |
| 乙车间 | 变红色 | 无明显现象 |
 根据固体物质M在水中的溶解度曲线图,回答下列问题:
根据固体物质M在水中的溶解度曲线图,回答下列问题: