题目内容
16. A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)
A、B、C、D、E均为初中化学常见物质,它们之间的转化关系如下图所示:(“→”表示某一种物质经一步反应可转化为另一种物质,部分生成物及反应条件已略去)(1)若A、C的组成元素相同,且常温下都是液体.D为一种常见的碱,则C为H2O(填化学式);A→C的化学反应基本类型为分解反应.
(2)若A为一种黑色固体,B、C的组成元素相同,D为一种常见的盐,则C为二氧化碳(填名称);写出D→E的化学反应方程式Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.(任写一种)
分析 (1)根据A、C的组成元素相同,且常温下都为液体,则A、C为水或过氧化氢,D为一种常见的碱,C能转化生成D,则C为水,A为过氧化氢进行分析;
(2)根据A为一种黑色固体,能转化生成B和C,B、C的组成元素相同,则A可能为碳,生成的B和C为一氧化碳或二氧化碳,D为一种常见的盐,C能转化生成D,则C为二氧化碳,B为一氧化碳,D可能为碳酸钠,碳酸钠能与氢氧化钙反应生成碳酸钙,碳酸钙能分解反应生成二氧化碳进行分析.
解答 解:(1)A、C的组成元素相同,且常温下都为液体,则A、C为水或过氧化氢,D为一种常见的碱,C能转化生成D,则C为水,A为过氧化氢,过氧化氢能分解生成水和氧气;
(2)A为一种黑色固体,能转化生成B和C,B、C的组成元素相同,则A可能为碳,生成的B和C为一氧化碳或二氧化碳,D为一种常见的盐,C能转化生成D,则C为二氧化碳,B为一氧化碳,D可能为碳酸钠,碳酸钠能与氢氧化钙反应生成碳酸钙,碳酸钙能分解反应生成二氧化碳,D→E的反应是碳酸钠和氢氧化钙反应生成碳酸钙沉淀和氢氧化钠,化学方程式为:Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
故答案为:(1)H2O,分解;
(2)二氧化碳,Na2CO3+Ca(OH)2═CaCO3↓+2NaOH.
点评 在解此类题时,首先将题中有特征的物质推出,然后结合推出的物质和题中的转化关系推导剩余的物质,最后将推出的各种物质代入转化关系中进行验证即可.

练习册系列答案
相关题目
6.化学与生活密切相关.下列说法正确的是( )
| A. | 晚上回家发现煤气泄漏,应开灯检查 | |
| B. | 合金、合成纤维、合成橡胶等都是重要的有机合成材料 | |
| C. | 少年儿童缺钙会患佝偻病或发育不良 | |
| D. | 用霉变的花生制成的花生油烹调食品 |
4.一定条件下密闭容器内发生了化学反应,反应前后各物质的质量变化如表所示,下列说法错误的是( )
| 物质 | A | B | C | D |
| 反应前的质量(克) | 17 | 64 | 2 | 0 |
| 反应后的质量(克) | m | 0 | 46 | 36 |
| A. | m=1 | B. | 反应生成的C与D的质量比为11:9 | ||
| C. | 该反应一定属于化合反应 | D. | 该反应可表示为:A+B→C+D |
1.下列有关金属的描述不正确的是( )
| A. | 地壳中含量最多的金属元素是铝 | |
| B. | 车船表面涂油漆可防止生锈 | |
| C. | 废铜屑可全部溶解于过量稀盐酸 | |
| D. | 用硫酸铜、石灰水配置农药波尔多液时,不能用铁制容器 |
5.几年前,广西河池宜州市境内龙江河发生了镉浓度超标事件.根据该事件某化学活动小组开展了一次关于金属镉与铜、银活动顺序的探究及镉污染事故处理方法的研讨活动.
查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;
②水体中镉元素通常以氯化镉的形式存在;
③氯化镉能溶于水,氢氧化镉难溶于水.
(一)金属镉与铜、银活动性顺序的探究
实验结论:活动性顺序:镉>铜>银
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为CdCl2+2NaOH═Cd(OH)2↓+2NaCl.小敏认为该方案虽然有效,但有缺陷,原因是烧碱具有强腐蚀性.受小聪与小敏启发,你认为可以用熟石灰(写俗称)代替烧碱.
查阅资料:①镉(Cd)是一种银白色金属,在化合物中通常表现为+2价;
②水体中镉元素通常以氯化镉的形式存在;
③氯化镉能溶于水,氢氧化镉难溶于水.
(一)金属镉与铜、银活动性顺序的探究
| 实验步骤 | 实验现象 | 实验结论 |
| 分别取适量镉、铜、银于试管中,加入足量稀盐酸 | 镉表面有气泡产生,铜、银表面无气泡产生 | 镉的活动性顺序大于铜与银 |
| 取适量铜于试管中,加入少量硝酸银溶液 | 铜表面析出了一层银白色物质, 溶液由无色变为蓝色. | 铜的活动性顺序大于银 |
(二)对镉污染事故处理方法的讨论
小聪认为可用向受污染河段抛撒过量烧碱固体的方法除去氯化镉,反应原理用化学方程式表示为CdCl2+2NaOH═Cd(OH)2↓+2NaCl.小敏认为该方案虽然有效,但有缺陷,原因是烧碱具有强腐蚀性.受小聪与小敏启发,你认为可以用熟石灰(写俗称)代替烧碱.
6.某兴趣小组同学为了寻找纯度超过85%的石灰石,对一样品进行了如下定量实验:
试通过分析计算:
(1)该实验中生成的二氧化碳的质量是4.4g.
(2)该石灰石样品的纯度是否符合要求?(该石灰石样品中杂质不与盐酸反应也不溶于水)
| 实验步骤 | ①称取烧杯的质量 | ②将适量盐酸加入烧杯中并称重 | ③称取少量石灰石样品加入烧杯中,使之与过量稀盐酸反应 | ④待反应完全后,称重 |
| 实验图示 | 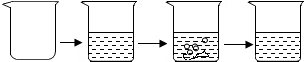 | |||
| 实验数据 | 烧杯的质量为50.0g | 烧杯和盐酸的质量为100.0g | 石灰石样品的质量为12.0g | 烧杯和其中剩余混合物的质量为107.6g |
(1)该实验中生成的二氧化碳的质量是4.4g.
(2)该石灰石样品的纯度是否符合要求?(该石灰石样品中杂质不与盐酸反应也不溶于水)
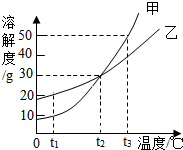 如图是甲、乙两种固体物质的溶解度曲线.t1℃时,将5g乙加到10g水中可得到12g溶液;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲;将t3℃时150g甲的饱和溶液稀释为20%,需加水100g.
如图是甲、乙两种固体物质的溶解度曲线.t1℃时,将5g乙加到10g水中可得到12g溶液;t3℃时,甲、乙各100g饱和溶液降温至t2℃,析出固体多的是甲;将t3℃时150g甲的饱和溶液稀释为20%,需加水100g.