题目内容
7.如图是实验室常用的装置,请回答有关问题:
(1)写出图中标号①仪器的名称:锥形瓶.
(2)实验室常用装置B与C组合来制取O2,发生反应的化学方程式为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑,收集氧气的最佳时机是当导管口有连续均匀气泡冒出时.
(3)利用B装置,甲同学用过氧化氢溶液和二氧化锰混合物制取O2,为了较好地控制反应速率,你认为该同学应将B中的长颈漏斗改为分液漏斗(填一种仪器名称).
(4)已知:NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑,乙同学想用该方法制取纯净的CO2,你认为合理的装置组合顺序为AFD(写字母序号).
分析 锥形瓶是常用的反应容器,分液漏斗可以控制反应的速率,制取装置包括加热和不需加热两种,如果用双氧水和二氧化锰制氧气就不需要加热,如果用高锰酸钾或氯酸钾制氧气就需要加热.氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集.实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热.二氧化碳能溶于水,密度比空气的密度大,因此只能用向上排空气法收集.用NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑制取纯净的CO2,要用浓硫酸除去氨气,再用向上排空气法收集.
解答 解:(1)锥形瓶是常用的反应容器,故答案为:锥形瓶;
(2)如果用双氧水和二氧化锰制氧气就不需要加热,过氧化氢在二氧化锰做催化剂的条件下生成水和氧气,要注意配平;氧气的密度比空气的密度大,不易溶于水,因此能用向上排空气法和排水法收集;用排水法收集较纯净氧气的适宜时间是:当导管口有连续均匀气泡冒出时;故答案为:2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑;当导管口有连续均匀气泡冒出时;
(3)分液漏斗可以控制反应的速率,故答案为:分液漏斗;
(4)用NH4HCO3$\frac{\underline{\;\;△\;\;}}{\;}$NH3↑+H2O+CO2↑制取纯净的CO2,要用浓硫酸除去氨气,再用向上排空气法收集,因为二氧化碳的密度比空气大;故答案为:AFD;
点评 本考点主要考查了仪器的名称、气体的制取装置和收集装置的选择,同时也考查了化学方程式的书写和注意事项等,综合性比较强.气体的制取装置的选择与反应物的状态和反应的条件有关;气体的收集装置的选择与气体的密度和溶解性有关.本考点是中考的重要考点之一,主要出现在实验题中.

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案| A. | 地壳中含量最高的金属元素是铜 | |
| B. | 石油炼制可得到汽油、煤焦油、航空煤油等 | |
| C. | 海洋中蕴藏着丰富的化学资源,海水中含有的化学元素有20多种 | |
| D. | 人们正在利用和开发的其他能源有氢能、太阳能、风能、地热能等 |
 近日,美国“信使”号水星探测器发现水星北极地区贮存着数十亿吨水冰(水为低温下固结的冰称为水冰),为人类探索水星提供了宝贵的科学资料,下列关于水冰的说法中正确的是( )
近日,美国“信使”号水星探测器发现水星北极地区贮存着数十亿吨水冰(水为低温下固结的冰称为水冰),为人类探索水星提供了宝贵的科学资料,下列关于水冰的说法中正确的是( )| A. | 水冰与水的化学性质不同 | B. | 构成水冰的分子不再运动 | ||
| C. | 氢、氧两种原子的个数比为2:1 | D. | 水冰和干冰是同一种物质 |


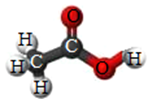 如图为某分子的结构模型,请回答下列问题:
如图为某分子的结构模型,请回答下列问题: 已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
已知空气的主要成分是氮气和氧气.某课外活动小组设计了测定空气中氧气含量的实验,实验装置如图所示:
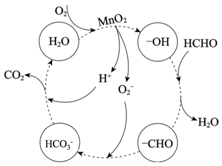 MnSO4在工业中有重要应用,可用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4.
MnSO4在工业中有重要应用,可用软锰矿浆(主要成分为MnO2和水,含有Fe2O3、FeO、Al2O3和少量PbO等杂质)浸出制备MnSO4.