题目内容
15. 如图为某分子的结构模型,请回答下列问题:
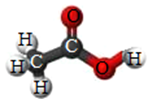
如图为某分子的结构模型,请回答下列问题:(1)该物质的碳、氢、氧原子个数比为1:2:1;
(2)该物质中碳元素的质量分数为40%.
分析 (1)由某分子的结构模型,1个分子是由2个碳原子、4个氢原子和2个氧原子构成的,进行分析解答.
(2)根据化合物中元素的质量分数的计算方法来分析.
解答 解:(1)由某分子的结构模型,1个分子是由2个碳原子、4个氢原子和2个氧原子构成的,其化学式为:C2H4O2.该物质的碳、氢、氧原子个数比为2:4:2=1:2:1;故填:1:2:1;
(2)该物质中碳元素的质量分数为$\frac{12×2}{12×2+1×4+16×2}×100%$=40%;故填:40.
点评 本题难度不大,考查同学们结合新信息、灵活运用化学式的含义与有关计算进行分析问题、解决问题的能力.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
3.关于Fe+2FeCl3═3X反应叙述合理的是( )
| A. | 该反应涉及的物质都是由原子构成的 | |
| B. | FeCl3中铁元素、氯元素的质量比为1:3 | |
| C. | X的化学式为FeCl2 | |
| D. | Fe中铁元素的化合价为+3 |
10.清洁的空气可以看做是一种气态的溶液,但是近年来北方不少地区多次受到沙尘暴袭击,天空中尘土飞扬,在这种情况出现时,空气可视为( )
| A. | 溶液 | B. | 纯净物 | C. | 乳浊液 | D. | 悬浊液 |
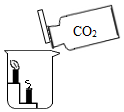
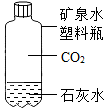
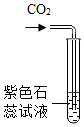
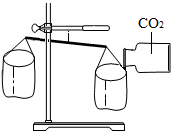

 某化学兴趣小组为了探究实验中敞口放置的氢氧化钠固体是否变质,进行了有关实验,如图所示.请你与他们一起完成以下探究活动:
某化学兴趣小组为了探究实验中敞口放置的氢氧化钠固体是否变质,进行了有关实验,如图所示.请你与他们一起完成以下探究活动: