题目内容
10.对比、分析、归纳是学习化学的重要方法.(1)已知H2、CO、C是初中化学常见的还原剂,请分析下列反应:
H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O 3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2 C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2
得出的结论是:物质(如H2、CO、C)作还原剂时,所含元素中,一定有元素的化合价在反应后升高(选填“升高”或“降低”或“不变”).
(2)依据上述结论,则在反应SO2+2H2S=3S+2H2O中作为还原剂的物质是H2S;该还原剂中所含元素化合价的变化是-2→0.
分析 氧化剂提供氧,化合价降低,具有氧化性,发生还原反应;还原剂得到氧,化合价升高,具有还原性,发生氧化反应.
解答 解:(1)在反应:H2+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+H2O,3CO+Fe2O3$\frac{\underline{\;高温\;}}{\;}$2Fe+3CO2,C+O2$\frac{\underline{\;点燃\;}}{\;}$CO2中物质H2、CO、C做还原剂,其中氢元素和碳元素的化合价升高了,所以三个反应还原剂中元素的化合价的变化规律还原剂在化学反应中元素化合价升高;即可得出结论:物质作还原剂时,所含元素中,一定有元素的化合价在反应后升高;
(2)依据上述结论,则在反应SO2+2H2S═3S+2H2O中,H2S中硫元素的化合价由-2价升高到0价,所以H2S是还原剂.
故答案为:(1)升高;(2)H2S,-2→0
点评 本题主要考查学生对课本知识掌握的熟练程度和总结规律的能力,属于基础知识的考查,对于化学方程式的考查是中考的一个重点.

练习册系列答案
 新课标阶梯阅读训练系列答案
新课标阶梯阅读训练系列答案
相关题目
1.下列物质间的转化,只有通过加入盐溶液才能一步实现的是( )
| A. | Fe→FeCl2 | B. | CuO→CuCl2 | C. | CaCO3→CaCl2 | D. | K2SO4→KCl |
18.现有CO2和CO的混合物30g,测得其中氧元素的质量分数为60%,将混合物通过足量的炙热氧化铜充分反应后,在通入足量的烧碱溶液中,让其充分反应,则生成碳酸钠的质量为 ( )
| A. | 100g | B. | 106g | C. | 96g | D. | 53g |
15.为测定某KClO3、KCl、MnO2的混合物中氯元素的质量分数,某同学把100g该混合物充分加热完全反应后,发现固体减少了4.8g,再将剩余固体完全溶于水经过滤洗涤干燥后称得黑色固体20.7g,则该混合物中氯元素的质量分数为( )
| A. | 45.5% | B. | 35.5% | C. | 25.5% | D. | 15.5% |
5.下列除杂(括号内为杂质)方法错误的是( )
| A. | CO(CO2):将气体通过澄清石灰水,然后干燥 | |
| B. | CO2(CO):将气体点燃 | |
| C. | 食盐(泥沙):溶解、过滤 | |
| D. | Cu(Fe):用磁铁吸引 |
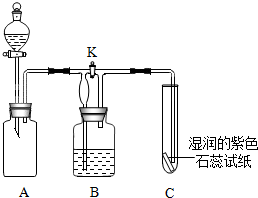 化学小组的同学利用如图所示的装置进行实验.回答相关问题:
化学小组的同学利用如图所示的装置进行实验.回答相关问题: 氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答:
氢氧化铜是一种常用的杀菌剂,常见的剂型有77%氢氧化铜可湿性粉剂、37.5%氢氧化铜悬浮剂、25%氢氧化铜悬浮剂.为了回收氢氧化铜,现向含CuCl2和HCl的100g混合溶液中,逐滴加溶质质量分数为10%的NaOH溶液,发生反应:CuCl2+2NaOH═2NaCl+Cu(OH)2↓.参加反应的NaOH溶液质量与生成沉淀质量关系如图.据图回答: