题目内容
6. 结合图回答下列问题.
结合图回答下列问题.(1)硫元素的质子数为:16;
(2)硫元素位于元素周期表的第三周期;
(3)B和C化学性质相似的原因是最外层电子数相同.
分析 (1)根据元素周期表的信息来分析;
(2)根据硫原子结构来分析;
(3)根据元素的化学性质跟它的原子的最外层电子数目关系非常密切,进行分析解答.
解答 解:(1)由硫元素周期表的信息可知,其原子序数为16,原子序数=核电荷数=核内质子数,故填:16;
(2)硫原子核外有三个电子层,在元素周期表中位于第三周期,故填:三;
(3)元素的化学性质跟它的原子的最外层电子数目关系非常密切,最外层电子数相同的元素化学性质相似,氧元素和硫元素化学性质相似的原因是它们的原子的最外层电子数相同.故填:最外层电子数相同.
点评 本题难度不大,考查学生对原子结构示意图及其意义的理解,了解原子结构示意图的意义是正确解题的关键.

练习册系列答案
相关题目
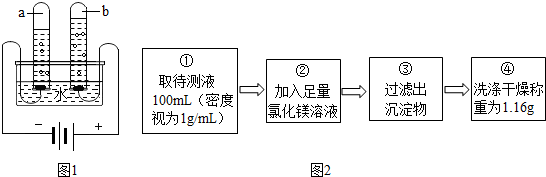
17.小华和小慧两位同学用分别如图1所示的装置进行电解水实验.该反应的化学方程式为2H2O$\frac{\underline{\;通电\;}}{\;}$2H2↑+O2↑.为了增强水的导电性,实验前小华向水中加入硫酸钠固体,则b试管中产生的气体是O2(填化学式),检验这种气体的方法是带火星木条.小慧在做实验时误将氯化钠当成硫酸钠加入水中,结果在检验b气体时闻到一股刺激性气味.在老师的指导下小华和小慧一起就这一异常现象开展了研究.
【定性研究】
Ⅰ.小慧猜想刺激性气味气体是氯化氢和氨气,小华测认为不一定是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老题指导下得知:
①食盐水是通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑
②氯气是种有刺激性气味的有毒气体.
由此可推测该刺激性气味的气体是氯气.
Ⅱ.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
小华则认为实验②不能确定一定有氯化钠,理由是①的反应中氯化铜和氢氧化钠反应,生成氯化钠和氢氧化铜,生成物中有氯化钠,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液,产生白色沉淀,所以不能证明原溶液中含有氯化钠.
【定量研究】
两位同学按如图2所示的实验步骤进行实验:
(1)步骤②加入氯化镁溶液必需足量,其目的是使氢氧化钠完全反应,滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;(写出实验步骤、现象和结论).
(2)计算等测液中氢氧化钠的质量分数(写出计算过程)
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)

【定性研究】
Ⅰ.小慧猜想刺激性气味气体是氯化氢和氨气,小华测认为不一定是氨气,理由是根据质量守恒定律,反应前后元素的种类不变,反应物中没有氮元素,所以不可能生成氨气.
在老题指导下得知:
①食盐水是通电时发生反应:2NaCl+2H2O$\frac{\underline{\;通电\;}}{\;}$↑NaOH+H2↑+Cl2↑
②氯气是种有刺激性气味的有毒气体.
由此可推测该刺激性气味的气体是氯气.
Ⅱ.为确定剩余溶液中的溶质,小慧进行如下实验,请帮她将实验报告补充完整.
| 实验操作 | 实验现象 | 实验结论 |
| ①取少量剩余溶液,滴入氯化铜溶液 | 产生蓝色絮状沉淀 | 溶液中含有氢氧化钠 |
| ②将①中反应后混合物过滤,向滤液中加入足量稀硝酸再滴入几滴硝酸银溶液 | 产生白色沉淀 | 溶液中含有氯化钠 |
【定量研究】
两位同学按如图2所示的实验步骤进行实验:
(1)步骤②加入氯化镁溶液必需足量,其目的是使氢氧化钠完全反应,滴加一定量氯化镁溶液后,判断所加氯化镁溶液是否的具体操作:静置,取上层溶液,滴加氢氧化钠溶液,如果产生白色沉淀,说明氯化镁过量,如果没有明显现象,说明氯化镁不过量;(写出实验步骤、现象和结论).
(2)计算等测液中氢氧化钠的质量分数(写出计算过程)
(3)若步骤④中缺少洗涤干燥的操作,所测定氢氧化钠的质量分数将偏大(选填“偏大”、“偏小”或“没影响”)
1.化学与人类健康关系密切.下列说法中,正确的是( )
| A. | 用甲醛的溶液保存海鲜产品 | B. | 人体缺钙元素容易患贫血病 | ||
| C. | 水果蔬菜能提供多种维生素 | D. | 霉变的大米淘洗煮熟可食用 |
18.人体内缺少可能导致骨骼疏松、畸形,但吸收过多会引起白内障的元素是( )
| A. | Zn | B. | I | C. | Ca | D. | Fe |
15. 如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略),下列说法错误的是( )
如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略),下列说法错误的是( )
 如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略),下列说法错误的是( )
如图表示了初中化学中一些常见物质的相互转化关系(部分反应条件已省略),下列说法错误的是( )| A. | 圈Ⅰ中发生的反应可能都是分解反应 | |
| B. | 利用反应①可制得烧碱 | |
| C. | 利用反应②可用来检验二氧化碳气体 | |
| D. | 圈Ⅱ中的化学反应说明氧气具有可燃性 |
16.实验室常用下列装置制取气体,请你根据所学知识回答下列问题.
(1)仪器a的名称是酒精灯.
(2)实验室制取氧气时,选用的收集装置是C(填字母序号).若改用如图I装置收集氧气、则气体应从b进(填“a”或“b”).
(3)实验室用B装置制取二氧化碳气体时,将生成的气体通入澄清石灰水中,未见变浑浊.为探究其原因,进行了如下过程:
【作出猜想】
A.石灰水已经完全变质;
B.气体中有挥发出来的HCl气体.
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色.于是排除了猜想A,你认为排除猜想A的理由是酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2.
②小明想探究所得气体中是否有挥发出来的HCl气体,设计如下实验.请你帮他完成实验,填写以下表格:
【查阅资料】
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为BHEC(填字母).

(1)仪器a的名称是酒精灯.
(2)实验室制取氧气时,选用的收集装置是C(填字母序号).若改用如图I装置收集氧气、则气体应从b进(填“a”或“b”).
(3)实验室用B装置制取二氧化碳气体时,将生成的气体通入澄清石灰水中,未见变浑浊.为探究其原因,进行了如下过程:
【作出猜想】
A.石灰水已经完全变质;
B.气体中有挥发出来的HCl气体.
【实验探究】
①取少量石灰水于试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到溶液变红色.于是排除了猜想A,你认为排除猜想A的理由是酚酞试液变红,说明溶液中存在碱性物质Ca(OH)2.
②小明想探究所得气体中是否有挥发出来的HCl气体,设计如下实验.请你帮他完成实验,填写以下表格:
| 实验步骤 | 实验现象 | 实验结论 |
| 气体中有HCl |
碳酸钠溶液中通入二氧化碳发生反应:Na2CO3+CO2+H2O═2NaHCO3
【拓展延伸】
如果用上述原料制得纯净的二氧化碳气体,所选仪器的连接顺序为BHEC(填字母).
