题目内容
2.小王同学对所学部分化学知识归纳如下,其中有错误的一组是( )| A.物质区别 | B.灭火方法 |
| 区分食盐水和蛋白质溶液--用饱和 (NH4)2SO4溶液 | 电器着火--切断电源,用液态二氧化碳灭火器灭火 |
| C.实验记录 | D.生活常识 |
| 用10ml量筒量取7.25mL水 | 用洗涤剂洗油污--乳化作用 |
| A. | 物质区别 | B. | 灭火方法 | C. | 实验记录 | D. | 生活常识 |
分析 A、饱和(NH4)2SO4的溶液,可使蛋白质的溶解度降低,而从溶液中析出;
B、电器着火,可以用液体二氧化碳灭火器;
C、量筒天平都是精确到0.1;
D、洗涤剂有乳化功能.
解答 解:A、向蛋白质水溶液中加入浓(NH4)2SO4的溶液,可使蛋白质的溶解度降低,而从溶液中析出,而食盐水没有这个现象,故A对
B、电器着火,可以用液体二氧化碳灭火器液态二氧化碳可以气化,不会留下痕迹.故B对
C、量筒只能精确到0.1ml,故不可能量取到7.25ml水,故C错
D、洗涤剂有乳化功能,能够出去油污.故D对
故选C.
点评 物质的性质决定了物质用途,解答本题时要充分了解物质的性质,只有理解了物质的性质,才能确定物质有哪些方面的用途.

练习册系列答案
相关题目
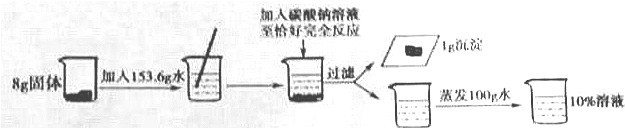
12.将含泥沙的粗盐提纯,并用制得的精盐配制80g 10%的食盐溶液.下列说法错误的是( )
| A. | 过滤时搅拌漏斗中的液体,可以加快过滤的速度 | |
| B. | 蒸发滤液时,不断用玻璃棒搅拌,防止液体溅出 | |
| C. | 配制溶液的步骤是:计算、称量、溶解 | |
| D. | 配制时需用的主要仪器有:天平、药匙、量筒、胶头滴管、烧杯、玻璃棒 |
17.空气中含量多且化学性质不活泼的气体是( )
| A. | 氮气 | B. | 二氧化碳 | C. | 氧气 | D. | 稀有气体 |
7.实验室里用如图所示装置还原氧化铁,关于该实验下列说法正确的是( )

| A. | 玻璃管中发生的反应属于置换反应 | |
| B. | 该实验只说明了一氧化碳具有还原性 | |
| C. | 实验观察到的现象为红棕色固体变黑,澄清石灰水变浑浊 | |
| D. | 实验时,通入纯净一氧化碳的同时,点燃酒精喷灯给玻璃管加热 |
14.KNO3和KCl在不同温度时的溶解度如下表所示.请回答下列问题:
(1)10℃时,131g KCl饱和溶液,蒸发10g水后再降温到10℃,可析出KCl晶体的质量为3.1g.
(2)将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采用的方法是②④(填序号).
①升高温度 ②加溶质KNO3 ③加水 ④恒温蒸发水
(3)KNO3溶液中含有少量NaCl时,可通过冷却热饱和溶液的方法提纯.对上述提纯后析出的晶体和剩余溶液描述正确的是A(填序号).
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离 D.析出的晶体中只含有KNO3
(4)氯化钾是一种钾肥.20℃时,欲测定某KCl溶液的pH,若先将pH试纸用蒸馏水润湿再进行测定,则所测得溶液的pH会不受影响(填“偏大”、“偏小”或“不受影响”).
| 温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | |
| 溶解度/g | KNO3 | 13.3 | 20.9 | 31.6 | 45.8 | 63.9 | 85.5 | 110 | 138 |
| KCl | 27.6 | 31.0 | 34.0 | 37.0 | 40.0 | 42.6 | 45.5 | 48.3 | |
(2)将一瓶接近饱和的硝酸钾溶液变成饱和溶液,可采用的方法是②④(填序号).
①升高温度 ②加溶质KNO3 ③加水 ④恒温蒸发水
(3)KNO3溶液中含有少量NaCl时,可通过冷却热饱和溶液的方法提纯.对上述提纯后析出的晶体和剩余溶液描述正确的是A(填序号).
A.剩余溶液一定是KNO3饱和溶液 B.剩余溶液一定是NaCl不饱和溶液
C.上述方法可以将两者完全分离 D.析出的晶体中只含有KNO3
(4)氯化钾是一种钾肥.20℃时,欲测定某KCl溶液的pH,若先将pH试纸用蒸馏水润湿再进行测定,则所测得溶液的pH会不受影响(填“偏大”、“偏小”或“不受影响”).
11.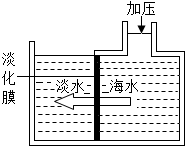 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
 淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )
淡化海水可采用膜分离技术(如图),水分子可以透过膜(海水中其他粒子不能透过)进入左侧的池子,从而得到淡水.以下分析中正确的是( )| A. | 这种膜可用滤纸代替 | B. | 左侧池中的淡水属于混合物 | ||
| C. | 右侧池中溶剂的质量减少 | D. | 右侧池中海水的溶质质量分数不变 |